Former brom en kation eller en anion?
Her er hvorfor:
* Elektronegativitet: Brom er en ikke -metal med en høj elektronegativitet. Dette betyder, at det har en stærk tendens til at få elektroner.
* Elektronkonfiguration: Bromin har 7 valenselektroner. Det har brug for endnu en elektron for at opnå en stabil oktetkonfiguration som den ædle gas krypton.
* ionisk binding: Brom accepterer let en elektron til dannelse af en bromidion (BR-), der har en -1 -ladning.
Derfor danner brom typisk en anion, ikke en kation.
Sidste artikelReaktion af aluminiumssulfat med bariumchlorid?
Næste artikelEr opløsning af ammoniumchlorid i vand en kemisk ændring?
 Varme artikler
Varme artikler
-
 Samling af store videnskabelige værktøjer til at kaste lys over fleksible proteinerL-R:ORNLs Arvind Ramanathan, Hugh ONeill, og Paul Gilna inde i Summit supercomputerrummet. Kredit:Oak Ridge National Laboratory Næsten et dusin videnskabsmænd på tværs af Oak Ridge National Labora
Samling af store videnskabelige værktøjer til at kaste lys over fleksible proteinerL-R:ORNLs Arvind Ramanathan, Hugh ONeill, og Paul Gilna inde i Summit supercomputerrummet. Kredit:Oak Ridge National Laboratory Næsten et dusin videnskabsmænd på tværs af Oak Ridge National Labora -
 Forskere måler elektronemission for at forbedre forståelsen af laserbaseret 3-D-tryk i metalForskere målte emission af elektroner fra overfladen af rustfrit stål under laserpulverbedfusion (LPBF) betingelser, demonstrere potentialet for at bruge termioniske emissionssignaler til at detekte
Forskere måler elektronemission for at forbedre forståelsen af laserbaseret 3-D-tryk i metalForskere målte emission af elektroner fra overfladen af rustfrit stål under laserpulverbedfusion (LPBF) betingelser, demonstrere potentialet for at bruge termioniske emissionssignaler til at detekte -
 ORNL opfylder FDA's vigtigste milepæl for kræftbekæmpende Ac-225 isotopMålrettet alfaterapi kan levere stråling til specifikke celler, med minimal indvirkning på omgivelserne, sunde celler. Kredit:Michelle Lehman og Jaimee Janiga/ORNL, US Department of Energy En sjæl
ORNL opfylder FDA's vigtigste milepæl for kræftbekæmpende Ac-225 isotopMålrettet alfaterapi kan levere stråling til specifikke celler, med minimal indvirkning på omgivelserne, sunde celler. Kredit:Michelle Lehman og Jaimee Janiga/ORNL, US Department of Energy En sjæl -
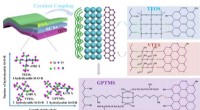 Silan regulerer termisk ledningsevne af kompositter på molekylært niveauFig. 1. Skematisk af PVA/fBN med forskellige SCA -koblinger. Kredit:CHENG Hua Et forskerhold fra Institute of Solid State Physics, Hefei Institutes of Physical Science har gennemført en undersøgel
Silan regulerer termisk ledningsevne af kompositter på molekylært niveauFig. 1. Skematisk af PVA/fBN med forskellige SCA -koblinger. Kredit:CHENG Hua Et forskerhold fra Institute of Solid State Physics, Hefei Institutes of Physical Science har gennemført en undersøgel
- Hvilken varmeoverførsel til faste stoffer?
- Nanoteknologi i kampen mod kræft
- Hvordan kan du genvinde saccharose af natriumchlorid, når det er opløst i vand?
- Hvad er bidraget fra Julius Lothar Meyer til periodisk bord?
- Hvad er hvert lag af jorden sammensat af?
- Hvilke partikler udgør et atom af selen-80?


