Ville du finde KF2 som en stabil forbindelse?
* Elektronegativitet: Kalium (K) er et meget elektropositivt element, hvilket betyder, at det let mister elektroner. Fluor (F) er meget elektronegativ, hvilket betyder, at det let får elektroner.
* ionisk binding: I KF2 skulle kalium miste to elektroner for at opnå en +2 ladning. Fluor, med kun en elektron -ledig stilling i sin ydre skal, kan kun acceptere en elektron.
* ionisk forhold: For at afbalancere ladningerne har du brug for to fluorioner (F-) for hver kaliumion (K+2). Imidlertid ville dette arrangement resultere i et ustabilt ionisk forhold.
Den stabile forbindelse med kalium og fluor er KF (kaliumfluorid). I denne forbindelse mister kalium en elektron for at blive K+, og fluor får en elektron til at blive F-. De resulterende ioniske ladninger er perfekt balance, hvilket skaber en stabil ionisk binding.
 Varme artikler
Varme artikler
-
 Øjne blinker på en chipDen nye hornhinde-på-en-chip-enhed kan gengive trykket fra bevægelige tårer inde i et blinkende øjenlåg, og kan mere præcist teste virkningerne af lægemidler på det menneskelige øje. Kredit:Mindy Taka
Øjne blinker på en chipDen nye hornhinde-på-en-chip-enhed kan gengive trykket fra bevægelige tårer inde i et blinkende øjenlåg, og kan mere præcist teste virkningerne af lægemidler på det menneskelige øje. Kredit:Mindy Taka -
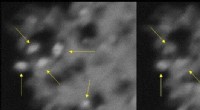 Usædvanlige nanopartikler kan gavne søgen efter at bygge en kvantecomputerPilene peger på, at titandioxid nanokrystaller lyser og blinker (venstre) og derefter falmer (højre). Kredit:Tewodros Asefa og Eliska Mikmekova Forestil dig små krystaller, der blinker som ildflue
Usædvanlige nanopartikler kan gavne søgen efter at bygge en kvantecomputerPilene peger på, at titandioxid nanokrystaller lyser og blinker (venstre) og derefter falmer (højre). Kredit:Tewodros Asefa og Eliska Mikmekova Forestil dig små krystaller, der blinker som ildflue -
 Kemisk jonglering med tre partiklerDr. Andreas Gansäuer og Anastasia Panfilova under epoxyhydrogenering på Kekulé Institute of Organic Chemistry and Biochemistry ved universitetet i Bonn. Kredit:Volker Lannert/Uni Bonn Kemikere fra
Kemisk jonglering med tre partiklerDr. Andreas Gansäuer og Anastasia Panfilova under epoxyhydrogenering på Kekulé Institute of Organic Chemistry and Biochemistry ved universitetet i Bonn. Kredit:Volker Lannert/Uni Bonn Kemikere fra -
 Robust MOF-materiale udviser selektive, fuldt reversibel og gentagelig opsamling af giftig atmosfær…Illustration af et nitrogendioxid-molekyle (afbildet i rødt og guld) indespærret i en pore i nanostørrelse af et MFM-300(Al) metal-organisk rammemateriale som karakteriseret ved brug af neutronspredni
Robust MOF-materiale udviser selektive, fuldt reversibel og gentagelig opsamling af giftig atmosfær…Illustration af et nitrogendioxid-molekyle (afbildet i rødt og guld) indespærret i en pore i nanostørrelse af et MFM-300(Al) metal-organisk rammemateriale som karakteriseret ved brug af neutronspredni


