Hvilket element har egenskaber og reaktiviteter, der mest ligner svovl?
Her er hvorfor:
* samme gruppe: Både svovl og selen hører til gruppe 16 (via) af den periodiske tabel, også kendt som chalcogens. Elementer i den samme gruppe har lignende kemiske egenskaber på grund af at have det samme antal valenselektroner.
* Lignende elektronkonfiguration: Svovl og selen har lignende elektronkonfigurationer i deres ydre skaller, hvilket stærkt påvirker deres reaktivitet.
* Lignende oxidation siger: Begge elementer kan udvise en række oxidationstilstande, herunder -2, +2, +4 og +6, hvilket fører til lignende typer forbindelser.
* ikke -metallisk karakter: Både svovl og selen er ikke -metaller, der deler egenskaber som dårlig ledningsevne og en tendens til at danne kovalente bindinger.
Mens andre elementer i gruppe 16 (ilt, tellurium og polonium) også deler ligheder med svovl, er selen den nærmeste analoge på grund af dens nærhed på det periodiske tabel.
Sidste artikelHvorfor ville natriumioner tiltrækkes af iltioner?
Næste artikelHvad er den strukturelle formel for en fosfatradikal?
 Varme artikler
Varme artikler
-
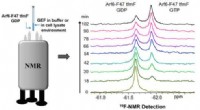 Hurtig metode hjælper med at detektere Arf6 guanin nukleotid udvekslingsfaktor aktivitet19 F NMR-baseret metode til Arf6 GEF aktivitet detektion. Kredit:Wu Bo Et forskerhold ledet af prof. Wang Junfeng fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabsakad
Hurtig metode hjælper med at detektere Arf6 guanin nukleotid udvekslingsfaktor aktivitet19 F NMR-baseret metode til Arf6 GEF aktivitet detektion. Kredit:Wu Bo Et forskerhold ledet af prof. Wang Junfeng fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabsakad -
 Nøglen til at sænke kuldioxidemissionerne er lavet af metalDe tilsyneladende rater for det ME-katalyserede malat (v0) under tilstanden NADPH, pyruvat, natriumbicarbonat og ME indeholdende aluminiumioner (røde). Kredit:Yutaka Amao, Osaka City University Ku
Nøglen til at sænke kuldioxidemissionerne er lavet af metalDe tilsyneladende rater for det ME-katalyserede malat (v0) under tilstanden NADPH, pyruvat, natriumbicarbonat og ME indeholdende aluminiumioner (røde). Kredit:Yutaka Amao, Osaka City University Ku -
 Undersøgelse beskriver cellulære fabrikker mere detaljeretKredit:CC0 Public Domain Mange vigtige naturlige produkter såsom antibiotika, immunsuppressiva og kræftlægemidler er afledt af mikroorganismer. Disse naturlige produkter er ofte små proteiner elle
Undersøgelse beskriver cellulære fabrikker mere detaljeretKredit:CC0 Public Domain Mange vigtige naturlige produkter såsom antibiotika, immunsuppressiva og kræftlægemidler er afledt af mikroorganismer. Disse naturlige produkter er ofte små proteiner elle -
 De kemiske hemmeligheder bag vanilje lokkerKredit:CC0 Public Domain Fra is til lattes er vanilje et af de mest populære krydderier i verden. Det er også en af de mest arbejdskrævende at producere, og genveje fører til et mindre velsmagend
De kemiske hemmeligheder bag vanilje lokkerKredit:CC0 Public Domain Fra is til lattes er vanilje et af de mest populære krydderier i verden. Det er også en af de mest arbejdskrævende at producere, og genveje fører til et mindre velsmagend
- Opløses blysulfat i vand?
- Jordens kappe, ikke dens kerne, kan have genereret planeter tidligt magnetfelt
- Beskriv hvad der sker langs en fejl under jordens surace, når der opstår et jordskælv?
- Hvilken fordel har Kelvin -skalaen til videnskabelige målinger?
- Hvor mange galakser er der i dit solsystem?
- Hvad er betegnelsen for en organisme med kromosombetegnelsen 3n?


