Hvad er den mindste enhed af en molekylær forbindelse med egenskaber, der forbinder?
Her er hvorfor:
* molekyler er de grundlæggende byggesten til molekylære forbindelser. De dannes, når to eller flere atomer binder sig kemisk sammen.
* egenskaber opstår fra arrangementet og interaktioner mellem atomer inden for et molekyle. Dette inkluderer ting som smeltepunkt, kogepunkt, reaktivitet og farve.
* Individuelle atomer udviser ikke de samme egenskaber som den forbindelse, de danner. For eksempel er et enkelt iltatom meget reaktivt, mens et molekyle af iltgas (O2) er relativt ureaktiv.
Eksempel:
Vand (H2O) er en molekylær forbindelse. Et enkelt molekyle vand har vandets egenskaber - det er en væske ved stuetemperatur, det er gennemsigtigt, det opløses mange stoffer osv. Du kan ikke nedbryde et vandmolekyle yderligere og stadig have vandets egenskaber.
Sidste artikelHvad er det formelle navn på sammensat H20?
Næste artikelSkadelige stoffer i luftvand eller jord kaldes?
 Varme artikler
Varme artikler
-
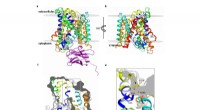 Karakterisering af strukturen af et medlem af L-Aminosyre Transporter (LAT) familienBasC transporterens opbygning. Kredit:Manuel Paladín, IRB Barcelona Hos mennesker, der er mere end 50 typer aminosyretransportører, som er ansvarlige for den cellulære optagelse af aminosyrer og f
Karakterisering af strukturen af et medlem af L-Aminosyre Transporter (LAT) familienBasC transporterens opbygning. Kredit:Manuel Paladín, IRB Barcelona Hos mennesker, der er mere end 50 typer aminosyretransportører, som er ansvarlige for den cellulære optagelse af aminosyrer og f -
 Lyser vejen til porøs elektronik og sensorerFig.1 Nanostruktur porøs titaniumoxid tynd film (TiOx) aflejret på plast (PI:polyimid) substratet. Kredit:Osaka University Mange almindelige husholdningsartikler og enheder har en belægning, der f
Lyser vejen til porøs elektronik og sensorerFig.1 Nanostruktur porøs titaniumoxid tynd film (TiOx) aflejret på plast (PI:polyimid) substratet. Kredit:Osaka University Mange almindelige husholdningsartikler og enheder har en belægning, der f -
 Rød, grøn, og blåt lys kan bruges til at kontrollere genekspression i manipuleret E. coliForskere fremstillede farvede billeder på kulturplader ved at bruge røde, grøn, og blåt lys til at kontrollere pigmentet produceret af bakterier med flerfarvesyn. Billedet er blevet farvekorrigeret i
Rød, grøn, og blåt lys kan bruges til at kontrollere genekspression i manipuleret E. coliForskere fremstillede farvede billeder på kulturplader ved at bruge røde, grøn, og blåt lys til at kontrollere pigmentet produceret af bakterier med flerfarvesyn. Billedet er blevet farvekorrigeret i -
 En brændstofkatalysator med højere udbytteKredit:Pixabay/CC0 Public Domain Oak Ridge National Laboratory-forskere har udviklet en ny katalysator til at omdanne ethanol til C3+ olefiner - de kemiske byggesten til vedvarende jetbrændstof og
En brændstofkatalysator med højere udbytteKredit:Pixabay/CC0 Public Domain Oak Ridge National Laboratory-forskere har udviklet en ny katalysator til at omdanne ethanol til C3+ olefiner - de kemiske byggesten til vedvarende jetbrændstof og
- Sådan beregnes vægten ved hjælp af tæthed og volumen
- Undervurder ikke bølgende grafen:Unik elektronik muliggjort af bølgede mønstre, der kanaliserer e…
- Hvordan den seneste økonomi holdt sorte, hvide unge voksne fra at forlade reden
- Hvad er kraft er lig med massetid?
- Isotoper er atomer med det samme element, der har forskellige atommasser?
- Kemikere skaber en kemisk sonde for bedre at forstå immunrespons


