Hvad giver kobber II -chlorid plus natriumphosphat?
Her er den afbalancerede kemiske ligning:
3 cucl₂ (aq) + 2 na₃po₄ (aq) → cu₃ (po₄) ₂ (s) + 6 NaCl (aq)
Her er hvad der sker:
* kobber (II) chlorid (Cucl₂) og natriumphosphat (Na₃po₄) er begge opløselige ioniske forbindelser, der adskiller sig i ioner i opløsning.
* kobber (II) ioner (cu²⁺) fra cucl₂ reager med fosfationer (po₄³⁻) Fra na₃po₄ til dannelse af kobber (II) phosphat (cu₃ (po₄) ₂) , som er et uopløseligt fast stof Det udfælder ud af opløsningen.
* natriumioner (NA⁺) Fra na₃po₄ reagerer med chloridioner (cl⁻) Fra Cucl₂ til dannelse af natriumchlorid (NaCl) , som forbliver opløst i opløsningen.
Nøgleobservationer:
* Reaktionen producerer en blågrøn bundfald af kobber (II) phosphat.
* Reaktionen er eksoterm , hvilket betyder, at det frigiver varme.
Bemærk: Denne reaktion bruges ofte i laboratoriet til at demonstrere dobbeltfortrængningsreaktioner og dannelsen af bundfald.
 Varme artikler
Varme artikler
-
 Adskillelse af gasser ved hjælp af fleksible molekylsigterMolekylærsigternes dynamiske natur og fleksibilitet er afgørende for at forstå deres ydeevne til transport af små molekyler. Kredit:University of Liverpool Forskere ved University of Liverpool og
Adskillelse af gasser ved hjælp af fleksible molekylsigterMolekylærsigternes dynamiske natur og fleksibilitet er afgørende for at forstå deres ydeevne til transport af små molekyler. Kredit:University of Liverpool Forskere ved University of Liverpool og -
 Usædvanlig koboltforbindelse udviklet til tyndfilmproduktionKredit:Pixabay/CC0 Public Domain Et forskerhold fra Ruhr-Universität Bochum (RUB) og Carleton University i Ottawa har fremstillet en roman, meget alsidig koboltforbindelse. Forbindelsens molekyler
Usædvanlig koboltforbindelse udviklet til tyndfilmproduktionKredit:Pixabay/CC0 Public Domain Et forskerhold fra Ruhr-Universität Bochum (RUB) og Carleton University i Ottawa har fremstillet en roman, meget alsidig koboltforbindelse. Forbindelsens molekyler -
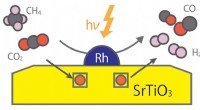 Miljøvenlig katalysator til omdannelse af metan til nyttige gasser ved hjælp af lys i stedet for v…Strontiumtitanat kombineret med rhodiumnanopartikler omdannede metan og kuldioxid til syntesegas under lysbestråling ved meget lavere temperaturer end dem, der kræves i termiske reaktorer. Kredit:Toky
Miljøvenlig katalysator til omdannelse af metan til nyttige gasser ved hjælp af lys i stedet for v…Strontiumtitanat kombineret med rhodiumnanopartikler omdannede metan og kuldioxid til syntesegas under lysbestråling ved meget lavere temperaturer end dem, der kræves i termiske reaktorer. Kredit:Toky -
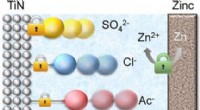 Zink-ion-hybridkondensatorer med ideelle anioner i elektrolytten viser ekstra lang ydelseKredit:Wiley Metal-ion hybrid kondensatorer kombinerer egenskaberne af kondensatorer og batterier. En elektrode bruger den kapacitive mekanisme, den anden redox-processer af batteritype. Forskere
Zink-ion-hybridkondensatorer med ideelle anioner i elektrolytten viser ekstra lang ydelseKredit:Wiley Metal-ion hybrid kondensatorer kombinerer egenskaberne af kondensatorer og batterier. En elektrode bruger den kapacitive mekanisme, den anden redox-processer af batteritype. Forskere
- Hvilke energiressourcer bruger varme fra under skorpe?
- SuperCam-instrument integreret på NASAs Mars 2020-rover
- Hvad er de tre elektriske apparater, der omdanner energi?
- Hvad er nogle former, som en videnskabelig model kan tage?
- Løbende kakerlakker, flagrende møl skaber en ny fysik af organismer
- Hvad er perioden med en bølge med hastighed 12 m s og frekvens 60 Hz?


