Bruges ammoniak i laboratoriet?
Her er en sammenbrud:
* formularer: I laboratorier opstår ammoniak typisk som:
* ammoniakgas (NH3): Dette er en farveløs gas med en skarp lugt.
* ammoniakopløsning (NH4OH): Dette er en opløsning af ammoniakgas i vand. Det kaldes ofte ammoniumhydroxid, men dette er ikke strengt nøjagtigt.
* ammoniumsalte (f.eks. Ammoniumchlorid, ammoniumsulfat): Dette er salte, der indeholder ammoniumion (NH4+).
Almindelige laboratorier:
* base: Ammoniakopløsning er en svag base og bruges i syre-base-reaktioner og titreringer.
* rengøring: Det er et godt rengøringsmiddel til glasvarer og udstyr på grund af dets evne til at opløse fedt og olier.
* reagens: Det er en reaktant i mange kemiske reaktioner, herunder produktion af gødning og farmaceutiske stoffer.
* buffer: Ammoniakopløsninger kan bruges til at fremstille buffere, som modstår ændringer i pH.
* spektroskopi: Ammoniumsalte anvendes i spektroskopi, især i nukleær magnetisk resonans (NMR) spektroskopi.
Sikkerhedshensyn:
* giftig og ætsende: Ammoniakgas er giftig og kan forårsage åndedrætsirritation. Ammoniakopløsning er også ætsende for hud og øjne.
* stærk lugt: Den skarpe lugt af ammoniak kan være overvældende.
* Korrekt håndtering: Arbejd altid med ammoniak i et godt ventileret område, bær passende personligt beskyttelsesudstyr (PPE) og følg ordentlige håndteringsprocedurer.
Det er vigtigt for:
* Butik ammoniakløsninger sikkert: I et godt ventileret område, væk fra varme og uforenelige stoffer.
* Brug forsigtighed, når du arbejder med ammoniak: Vær opmærksom på dets farer og tag de nødvendige forholdsregler.
* Følg laboratoriesikkerhedsretningslinjer: Konsulter altid dine laboratoriets sikkerhedsprotokoller og retningslinjer for korrekt håndtering og bortskaffelse.
I resuméet Ammoniak er et alsidigt kemikalie med mange anvendelser i laboratorier. Det er dog vigtigt at være opmærksom på dets farer og håndtere det med omhu.
Sidste artikelHvad vil der ske, hvis du kombinerer fast og flydende?
Næste artikelHvilket er ikke sandt om den kemiske formel for stoffer?
 Varme artikler
Varme artikler
-
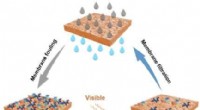 Forskere udvikler N-dopede selvrensende membraner, der bruger bestråling af synligt lysSkematisk diagram af N-TiO 2 og TiO 2 overtrukket membranforberedelse og mekanisme for synligt lysaktiveret fotokatalyse til begroningsbegrænsning. Kredit:ZHANG Huiru Forskere fra Institute of
Forskere udvikler N-dopede selvrensende membraner, der bruger bestråling af synligt lysSkematisk diagram af N-TiO 2 og TiO 2 overtrukket membranforberedelse og mekanisme for synligt lysaktiveret fotokatalyse til begroningsbegrænsning. Kredit:ZHANG Huiru Forskere fra Institute of -
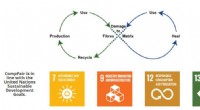 Selvhelbredende kompositter forlænger produktets levetidKredit:CompPair Næsten 20 millioner tons polymerkompositmaterialer produceres hvert år verden over, og markedet vokser med omkring 5% årligt. Det er ifølge JEC, en international sammensætningsindu
Selvhelbredende kompositter forlænger produktets levetidKredit:CompPair Næsten 20 millioner tons polymerkompositmaterialer produceres hvert år verden over, og markedet vokser med omkring 5% årligt. Det er ifølge JEC, en international sammensætningsindu -
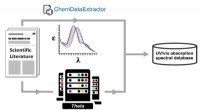 Automatisk databaseoprettelse til materialeopdagelse:Innovation fra frustrationAutogenerering af en ultraviolet-synlig (UV-vis) absorptionsspektral database via en dobbelt eksperimentel og beregningsmæssig kemisk datavej ved hjælp af ALCFs Theta-supercomputer. Kredit:Jacqueline
Automatisk databaseoprettelse til materialeopdagelse:Innovation fra frustrationAutogenerering af en ultraviolet-synlig (UV-vis) absorptionsspektral database via en dobbelt eksperimentel og beregningsmæssig kemisk datavej ved hjælp af ALCFs Theta-supercomputer. Kredit:Jacqueline -
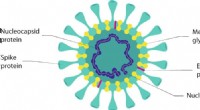 Antivirale overflader, overfladebelægninger og deres virkningsmekanismerFig. 1:Skematisk over en virusstruktur baseret på coronavirus. Kredit: Kommunikationsmaterialer (2021). DOI:10.1038/s43246-021-00153-y Forskere fra The National Physical Laboratory (NPL) og Natio
Antivirale overflader, overfladebelægninger og deres virkningsmekanismerFig. 1:Skematisk over en virusstruktur baseret på coronavirus. Kredit: Kommunikationsmaterialer (2021). DOI:10.1038/s43246-021-00153-y Forskere fra The National Physical Laboratory (NPL) og Natio
- Hvilken planet repræsenterer fredag?
- Hvad er de generelle formler for gruppe 1 metaloxider?
- Marine hedebølger bliver varmere, holder længere og gør mere skade
- Det amerikanske militær har officielt offentliggjort tre UFO-videoer. Hvorfor er der ikke nogen, de…
- Hvordan er det muligt, at du kan spise natrium og klor i en forbindelse sammen, når de er farlige e…
- Forskerhold udvikler ny højtydende fotoelektrode, der bruger zinkoxid nanopagoda-array


