En opløsning af ammoniak tilsættes til et jernchlorid?
reaktionen:
* jernioner (Fe³⁺) reagerer med ammoniak (NH₃) for at danne en kompleks ion kaldet hexaammineiron (III) ion [Fe (NH₃) ₆] ³⁺:
Fe³⁺ (aq) + 6nh₃ (aq) → [Fe (NH₃) ₆] ³⁺ (aq)
* [Fe (NH₃) ₆] ³⁺ Ion hydrolyseres derefter i vand, hvilket resulterer i frigivelse af H⁺ioner og dannelse af et hydroxidforstyrrende (Fe (OH) ₃):
[Fe (NH₃) ₆] ³⁺ (aq) + 3H₂O (L) → Fe (OH) ₃ (S) + 6NH₄⁺ (AQ)
Resultatet:
* Det observerede rødbrune bundfald er ferrisk hydroxid (Fe (OH) ₃) .
* Opløsningen indeholder også ammoniumioner (NH₄⁺).
Yderligere noter:
* Mængden af tilsat ammoniak bestemmer resultatet.
* Hvis ammoniak tilsættes i overskydende, kan bundfaldet opløses for at danne en farveløs opløsning, der indeholder [Fe (NH₃) ₆] ³⁺ -kompleksionen.
* Reaktionen er et eksempel på en kompleksationsreaktion, hvor en metalion danner et kompleks med ligander (i dette tilfælde ammoniakmolekyler).
* Dannelsen af bundfaldet er en reversibel reaktion. Tilsætning af syre kan genudvikle bundfaldet ved at skifte ligevægt mod dannelsen af [Fe (NH₃) ₆] ³⁺.
Denne reaktion er en almindelig laboratorietest for tilstedeværelsen af ferriske ioner.
 Varme artikler
Varme artikler
-
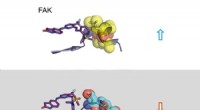 Når aktivt stof og målprotein omfavner hinandenØverste del:Lang opholdstid. En inhibitor (til venstre:stick -model) binder sig til signalmolekylet FAK (til højre:en del af FAK -proteinet afbildet som calottemodel med kugler). Strukturændringen af
Når aktivt stof og målprotein omfavner hinandenØverste del:Lang opholdstid. En inhibitor (til venstre:stick -model) binder sig til signalmolekylet FAK (til højre:en del af FAK -proteinet afbildet som calottemodel med kugler). Strukturændringen af -
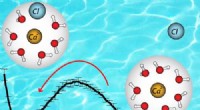 Udforskning af forholdet mellem to-kroppen og kollektivetDen frie energi er forskellig mellem ionparret (venstre) og ionen alene (højre). Det var ikke muligt at se denne forskel med tidligere tilgange. Kredit:American Chemical Society Fra batterier til
Udforskning af forholdet mellem to-kroppen og kollektivetDen frie energi er forskellig mellem ionparret (venstre) og ionen alene (højre). Det var ikke muligt at se denne forskel med tidligere tilgange. Kredit:American Chemical Society Fra batterier til -
 Sporing af laboratoriedyrket væv med lysEn tom petriskål med to optiske fibre, illustrerer en version af forskernes eksperiment. Den venstre fiber (normalt skinnende infrarødt lys, men afbildet her som synligt rødt lys) er en temperatursens
Sporing af laboratoriedyrket væv med lysEn tom petriskål med to optiske fibre, illustrerer en version af forskernes eksperiment. Den venstre fiber (normalt skinnende infrarødt lys, men afbildet her som synligt rødt lys) er en temperatursens -
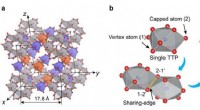 Gennembrud mod løsning af glasets strukturelle mysterium(a) Røde kugler er Pd- og Ni -atomer, hvorimod de blå kugler repræsenterer P -atomer. Den orangefarvede polyeder repræsenterer den Pd-berigede lille klynge, og det blåfarvede polyeder repræsenterer de
Gennembrud mod løsning af glasets strukturelle mysterium(a) Røde kugler er Pd- og Ni -atomer, hvorimod de blå kugler repræsenterer P -atomer. Den orangefarvede polyeder repræsenterer den Pd-berigede lille klynge, og det blåfarvede polyeder repræsenterer de
- Hvilke kræfter bruges i et ballon- og raketlaboratorium?
- Hvordan adskiller bjergene sig i Pacific Ring of Fire fra Fold Mountains?
- Hvilket vejr er forbundet med stratusskyer?
- Hvilke obligationer overfører elektroner?
- Hvad er en forstyrrelse, der bærer energi, men ikke betyder noget fra et sted til et andet?
- Hvordan bruges syre i maling?


