Hvad er ligningen til fremstilling af sæbe fra stearinsyre og natriumhydroxid?
c₁₇h₃₅cooh (stearinsyre) + NaOH (natriumhydroxid) → c₁₇h₃₅coona (natriumstearat) + H₂O (vand)
Her er en sammenbrud:
* stearinsyre (c₁₇h₃₅cooh): Dette er en langkædede fedtsyre, der er den primære komponent i mange fedtstoffer og olier.
* natriumhydroxid (NaOH): Dette er en stærk base, der ofte bruges til sæbefremstilling.
* natriumstearat (c₁₇h₃₅coona): Dette er sæbe -molekylet. Natriumionen (Na⁺) danner en ionisk binding med carboxylatgruppen (-coo⁻) af stearinsyremolekylet.
* vand (H₂O): Dette er et biprodukt af reaktionen.
mekanisme:
Reaktionen mellem stearinsyre og natriumhydroxid er en saponification reaktion. Dette er en type hydrolysereaktion, hvor en ester (i dette tilfælde esterbindingen i stearinsyre) nedbrydes af en stærk base.
1.
2. esterbindingen går i stykker, danner en carboxylation (rcoo⁻) og vand.
3.
Bemærk:
* Dette er en forenklet ligning. I virkeligheden er reaktionen mere kompleks og involverer flere trin.
* Reaktionen udføres typisk i en varm opløsning og involverer ofte andre fedtstoffer eller olier ud over stearinsyre.
* SOAP-molekylet har et polært (hydrofil) hoved (carboxylatgruppen) og en ikke-polær (hydrofob) hale (den lange carbonhydridkæde). Denne struktur tillader sæbe at fungere som et overfladeaktivt middel, hvilket betyder, at den kan sænke overfladespændingen af vand og hjælpe med at emulere snavs og fedt.
 Varme artikler
Varme artikler
-
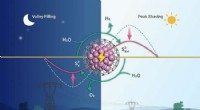 Meget effektive ringbrynjekatalysatorer udviklet til afkoblet vandelektrolyseEffektiv afkoblet vandelektrolyseanordning realiserede peak barbering og dalfyldning af elektricitet. Kredit:ZHANG Mo Afkoblet elektrolyse af vand er en lovende strategi for spidsbelastningsregule
Meget effektive ringbrynjekatalysatorer udviklet til afkoblet vandelektrolyseEffektiv afkoblet vandelektrolyseanordning realiserede peak barbering og dalfyldning af elektricitet. Kredit:ZHANG Mo Afkoblet elektrolyse af vand er en lovende strategi for spidsbelastningsregule -
 Forskere finder en billigere måde at oplyse OLED-skærme påKemiker Mark E. Thompson har nye kobberbaserede lysdioder opfundet af ham og et team af kemikere, der kunne være en billigere løsning for tv- og smartphone-skærme til at producere farven-herunder blå-
Forskere finder en billigere måde at oplyse OLED-skærme påKemiker Mark E. Thompson har nye kobberbaserede lysdioder opfundet af ham og et team af kemikere, der kunne være en billigere løsning for tv- og smartphone-skærme til at producere farven-herunder blå- -
 At se kemiske reaktioner med musik(Top) Lydkontrollerede spatiotemporale mønstre. Skematisk repræsentation af eksperimentel opsætning brugt til lydstyret spatiotemporal mønstergenerering. For mønstergenereringseksperimenter, O2-følsom
At se kemiske reaktioner med musik(Top) Lydkontrollerede spatiotemporale mønstre. Skematisk repræsentation af eksperimentel opsætning brugt til lydstyret spatiotemporal mønstergenerering. For mønstergenereringseksperimenter, O2-følsom -
 Kunstig tunge kan skelne mellem whiskyKredit:University of Glasgow Forskere afslørede tirsdag, at de er kommet med en kunstig tunge, der kan skelne subtile forskelle mellem whisky. Eksperter ved University of Glasgow har bygget miniat
Kunstig tunge kan skelne mellem whiskyKredit:University of Glasgow Forskere afslørede tirsdag, at de er kommet med en kunstig tunge, der kan skelne subtile forskelle mellem whisky. Eksperter ved University of Glasgow har bygget miniat
- Hvordan kvantematerialer snart kan gøre Star Trek-teknologi til virkelighed
- Er kontinentale kløft placeret vest for Appalachian Mountains?
- Finjustering af magnetisk spin for hurtigere, mindre hukommelsesenheder
- Hvor mange mol platin er der i 26,4 pt?
- Hvad er formlen for natriumethanoat?
- Det sydlige Californiens flammer viser tegn på afmatning


