Er fluor og klor en ionisk binding?
* Elektronegativitet: Både fluor og klor er meget elektronegative elementer. Dette betyder, at de har en stærk tendens til at tiltrække elektroner.
* Lignende elektronegativitet: Mens fluor er det mest elektronegative element, er klor også meget elektronegativ. Deres elektronegativitetsforskel er ikke stor nok til at forårsage en komplet overførsel af elektroner, hvilket er nødvendigt for en ionisk binding.
* kovalent binding: På grund af deres lignende elektronegativitet vil fluor og klor dele elektroner for at danne en kovalent binding. Dette skyldes, at hverken atom har et stærkt nok træk til at tage et elektron helt fra det andet.
Kortfattet: Elektronegativitetsforskellen mellem fluor og klor er ikke signifikant nok til at danne en ionisk binding. I stedet deler de elektroner til dannelse af en kovalent binding.
Sidste artikelHvor mange elektroner er gaver i fluoratom?
Næste artikelHvordan beskriver du farven på Mineral Topaz?
 Varme artikler
Varme artikler
-
 Brug af kunstig intelligens til at lugte roserneAnandasankar Ray er professor i molekylær, celle- og systembiologi ved UC Riverside. Kredit:L. Duka. Et par forskere ved University of California, Riverside, har brugt maskinlæring til at forstå,
Brug af kunstig intelligens til at lugte roserneAnandasankar Ray er professor i molekylær, celle- og systembiologi ved UC Riverside. Kredit:L. Duka. Et par forskere ved University of California, Riverside, har brugt maskinlæring til at forstå, -
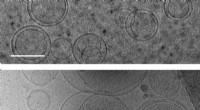 De første celler kan være opstået, fordi byggesten af proteiner stabiliserede membranerBilleder af membraner (cirkler) taget ved hjælp af transmissionselektronkryomikroskopi. Øverst:membraner i en opløsning, der ikke indeholder aminosyrer. Nederst:membraner i en opløsning indeholdende s
De første celler kan være opstået, fordi byggesten af proteiner stabiliserede membranerBilleder af membraner (cirkler) taget ved hjælp af transmissionselektronkryomikroskopi. Øverst:membraner i en opløsning, der ikke indeholder aminosyrer. Nederst:membraner i en opløsning indeholdende s -
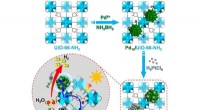 Enkeltatomlegering:Fremragende cokatalysator til fotokatalyseOverfladeladningstilstanden af co-katalysator spiller en vigtig rolle i fotokatalyse. Imidlertid, forordningen om overfladeladningstilstand for co-katalysatorer, især ved at ændre deres mikrostruktu
Enkeltatomlegering:Fremragende cokatalysator til fotokatalyseOverfladeladningstilstanden af co-katalysator spiller en vigtig rolle i fotokatalyse. Imidlertid, forordningen om overfladeladningstilstand for co-katalysatorer, især ved at ændre deres mikrostruktu -
 Kemikere bruger elektrokemi til at forstærke lægemiddelproduktionenPostdoc Niankai Fu, hovedforfatter til Science -papiret. Kredit:Cornell University Giv din medicin et stød. Ved at bruge - elektrokemi - en teknik, der kombinerer elektricitet og kemi, fremtidige
Kemikere bruger elektrokemi til at forstærke lægemiddelproduktionenPostdoc Niankai Fu, hovedforfatter til Science -papiret. Kredit:Cornell University Giv din medicin et stød. Ved at bruge - elektrokemi - en teknik, der kombinerer elektricitet og kemi, fremtidige
- Er gasser, der afgives af vulkanermineraler?
- Ultrahurtig fjernbetjening af lysudsendelse
- Cellevæg: Definition, struktur og funktion (med diagram)
- Hvis du ville lære mere om gammel videnskabelig viden, hvis liv ville undersøge?
- Ingeniører hacker cellebiologi for at skabe 3D-former fra levende væv
- Videnskabsprojekter på magneter til tredie gradere


