Hvor mange hydrogenatomer ville et boratom have brug for at danne kovalent binding med det, så det er stabilt?
Her er hvorfor:
* Borons elektronkonfiguration: Bor har et atomnummer på 5, hvilket betyder, at det har 5 elektroner. Dens elektronkonfiguration er 1S² 2S²2P¹.
* Valenselektroner: Bor har tre elektroner i sin yderste (valence) shell (2S²2P¹).
* octet regel: Atomer har en tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration af otte elektroner i deres valensskal (Octet -reglen).
* Borons stabilitet: Bor kan opnå stabilitet ved at dele sine tre valenselektroner med tre brintatomer og danne tre kovalente bindinger. Dette skaber et molekyle af boran (BH₃), hvor bor har en fuld ydre skal af seks elektroner.
Derfor har et boratom brug for tre hydrogenatomer for at danne kovalente bindinger og opnå en stabil elektronkonfiguration.
Sidste artikelHvad er den kemiske formel for fluordas?
Næste artikelHvad giver natrium plus brint?
 Varme artikler
Varme artikler
-
 Kemisk syntese med kunstig intelligens:Forskere udvikler ny computermetodeKredit:CC0 Public Domain I 1996 da en computer vandt en kamp mod den regerende verdensmester i skak, Garry Kasparov, det var intet mindre end en fornemmelse. Efter dette gennembrud i skakverdenen,
Kemisk syntese med kunstig intelligens:Forskere udvikler ny computermetodeKredit:CC0 Public Domain I 1996 da en computer vandt en kamp mod den regerende verdensmester i skak, Garry Kasparov, det var intet mindre end en fornemmelse. Efter dette gennembrud i skakverdenen, -
 Forskere rekonstruerer de biokemiske mekanismer ved fotosynteseKredit:CC0 Public Domain Ansvarlig for planternes grønne farve, de væsentlige mekanismer for fremkomsten af fotosyntese er netop blevet undersøgt på niveau med planteceller. Forskere fra univers
Forskere rekonstruerer de biokemiske mekanismer ved fotosynteseKredit:CC0 Public Domain Ansvarlig for planternes grønne farve, de væsentlige mekanismer for fremkomsten af fotosyntese er netop blevet undersøgt på niveau med planteceller. Forskere fra univers -
 Upcycling af plastikposer til batterideleKredit:American Chemical Society Plastposeforurening er blevet et stort miljøproblem, får nogle byer og lande til at beskatte eller forbyde sækkene kraftigt. Men hvad nu hvis brugte plastikposer k
Upcycling af plastikposer til batterideleKredit:American Chemical Society Plastposeforurening er blevet et stort miljøproblem, får nogle byer og lande til at beskatte eller forbyde sækkene kraftigt. Men hvad nu hvis brugte plastikposer k -
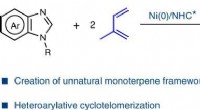 Forskere indser nikkel-katalyseret asymmetrisk heteroarylativ cyclotelomerisering af isoprenGrafisk abstrakt. Kredit:Nature Catalysis (2022). DOI:10.1038/s41929-022-00825-z Isopren bruges som en forløber til at producere terpener og terpenoider. Den direkte katalytiske omdannelse af isopr
Forskere indser nikkel-katalyseret asymmetrisk heteroarylativ cyclotelomerisering af isoprenGrafisk abstrakt. Kredit:Nature Catalysis (2022). DOI:10.1038/s41929-022-00825-z Isopren bruges som en forløber til at producere terpener og terpenoider. Den direkte katalytiske omdannelse af isopr
- Kabelbakterier kan drastisk reducere udledningen af drivhusgasser fra risdyrkning
- Hvad er praksis uden videnskabelige baser?
- Hvilken af de store observatorier var den første, der blev lanceret, og indsamler stadig oplysnin…
- Hvad er meningen med fysiske faciliteter?
- Hvad er opregning i mikrobiologi?
- Har alle molekyler varmeenergi?


