Hvad er reaktion af jern III -hydroxid plus fosforsyre?
Her er den afbalancerede kemiske ligning:
Fe (OH) ₃ (s) + H₃po₄ (aq) → fepo₄ (s) + 3H₂O (l)
Forklaring:
* jern (III) hydroxid (Fe (OH) ₃) er et solidt, brunt bundfald.
* fosforsyre (H₃po₄) er en farveløs, ætsende væske.
* jern (III) phosphat (fepo₄) er et gult, uopløseligt fast stof.
* vand (H₂O) er en væske.
mekanisme:
Reaktionen involverer overførsel af protoner (H⁺) fra fosforsyren til hydroxidionerne (OH⁻) i jern (III) hydroxid. Denne neutraliseringsreaktion danner vand og jern (III) phosphat, som udfældes ud af opløsningen som et gult fast stof.
Observationer:
* Når fosforsyre tilsættes til jern (III) hydroxid, dannes et gult bundfald af jern (III) phosphat.
* Reaktionen frigiver varme, hvilket indikerer, at den er eksoterm.
Bemærk:
Reaktionen kan udføres i laboratorieindstillinger. Det er dog vigtigt at håndtere fosforsyre med omhu, da det er ætsende.
 Varme artikler
Varme artikler
-
 grafen, perovskites, og silicium – en ideel tandem til effektive solcellerDenne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Forskere ved universitetet i Rom Tor Vergata, det italienske teknologiske institut (IIT) og dets
grafen, perovskites, og silicium – en ideel tandem til effektive solcellerDenne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Forskere ved universitetet i Rom Tor Vergata, det italienske teknologiske institut (IIT) og dets -
 Kulstofaffald fra stålproduktion kan genanvendes til nye produkterFigur 1:At vide, hvordan en nikkeljernsulfidkatalysator hjælper med at reducere kuldioxid til kulilte og andre kulbaserede produkter, kan føre til teknologier, der kan omdanne kuldioxid i atmosfæren t
Kulstofaffald fra stålproduktion kan genanvendes til nye produkterFigur 1:At vide, hvordan en nikkeljernsulfidkatalysator hjælper med at reducere kuldioxid til kulilte og andre kulbaserede produkter, kan føre til teknologier, der kan omdanne kuldioxid i atmosfæren t -
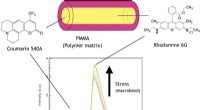 Polymerbaseret optisk fiber til visualisering af materialespændingOvergang af outputspektrum af en fluorophor-doteret polymer optisk fiber ved påført belastning. Kredit:University of Electro Communications Fiberoptisk strain sensing er kendt for sin evne til at
Polymerbaseret optisk fiber til visualisering af materialespændingOvergang af outputspektrum af en fluorophor-doteret polymer optisk fiber ved påført belastning. Kredit:University of Electro Communications Fiberoptisk strain sensing er kendt for sin evne til at -
 Succesfuld syntese af nanomateriale, der forbedrer katalysatorens effektivitet(Venstre mod højre) Dr. Md Shahriar Hossain, Prof Yusuke Yamauchi og Dr. Katy Wood ved Quokka-instrumentet. Kredit:Australian Nuclear Science and Technology Organisation (ANSTO) Et stort internati
Succesfuld syntese af nanomateriale, der forbedrer katalysatorens effektivitet(Venstre mod højre) Dr. Md Shahriar Hossain, Prof Yusuke Yamauchi og Dr. Katy Wood ved Quokka-instrumentet. Kredit:Australian Nuclear Science and Technology Organisation (ANSTO) Et stort internati
- Hvilken styrke forhindrer bjerge i at synke ned i mantlen?
- Antistoffer fra ørkenen som guider til syge celler
- Hvorfor Månen ikke har noget lys?
- Utilsigtet konsekvens af COVID-19:cybermobning kan øges
- På jagt efter superjord:Spectrograph CRIRES+ ved ESOs Very Large Telescope
- Hvilket er det mest almindelige molekyle i M -stjerner?


