Er en svovlfluorbinding polar?
* Elektronegativitetsforskel: Fluor (F) er det mest elektronegative element på den periodiske tabel, mens svovl (er) har en signifikant lavere elektronegativitet. Dette betyder, at fluor tiltrækker de delte elektroner i bindingen stærkere end svovl.
* Polaritet: Den ujævne deling af elektroner skaber en delvis negativ ladning (Δ-) på fluoratomet og en delvis positiv ladning (Δ+) på svovlatomet. Denne adskillelse af ladning inden for bindingen er det, der definerer en polær binding.
Kortfattet: Den store elektronegativitetsforskel mellem svovl og fluor fører til en polær S-F-binding.
Sidste artikelHvad har brintperoxid i det?
Næste artikelHvordan er mekanisk forvitring og kemisk forskellig?
 Varme artikler
Varme artikler
-
 Ny polymermembranteknologi forbedrer effektiviteten af kuldioxidopsamlingKredit:Unsplash/CC0 Public Domain Forskere har udviklet en ny membranteknologi, der muliggør mere effektiv fjernelse af kuldioxid (CO2 ) fra blandede gasser, såsom emissioner fra kraftværker. For
Ny polymermembranteknologi forbedrer effektiviteten af kuldioxidopsamlingKredit:Unsplash/CC0 Public Domain Forskere har udviklet en ny membranteknologi, der muliggør mere effektiv fjernelse af kuldioxid (CO2 ) fra blandede gasser, såsom emissioner fra kraftværker. For -
 Forskning i perovskit-silicium tandemceller viser ny vej at gåNREL-forskerne Chuanxiao Xiao (til venstre) og Kai Zhu samarbejdede med forskere fra Republikken Korea for at validere potentialet af perovskit-silicium tandem solceller til at opnå mere end 30 % effe
Forskning i perovskit-silicium tandemceller viser ny vej at gåNREL-forskerne Chuanxiao Xiao (til venstre) og Kai Zhu samarbejdede med forskere fra Republikken Korea for at validere potentialet af perovskit-silicium tandem solceller til at opnå mere end 30 % effe -
 Ultralyd kan lave stærkere 3D-trykte legeringer3D -printede titaniumlegeringer under et elektronmikroskop:prøve til venstre med store, langstrakte krystaller blev trykt konventionelt, mens prøve til højre med finere, kortere krystaller blev trykt
Ultralyd kan lave stærkere 3D-trykte legeringer3D -printede titaniumlegeringer under et elektronmikroskop:prøve til venstre med store, langstrakte krystaller blev trykt konventionelt, mens prøve til højre med finere, kortere krystaller blev trykt -
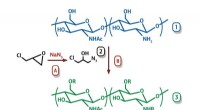 Kemikere får nyt materiale til antibakterielle madbelægningerRUDN University kemikere har udviklet en enkel og bekvem metode til fremstilling af derivater af den naturlige polymer chitosan. Disse derivater er ugiftige og har en udtalt antibakteriel aktivitet på
Kemikere får nyt materiale til antibakterielle madbelægningerRUDN University kemikere har udviklet en enkel og bekvem metode til fremstilling af derivater af den naturlige polymer chitosan. Disse derivater er ugiftige og har en udtalt antibakteriel aktivitet på


