Hvad er reaktionen af calciumhydroxid og nitrosyre?
Her er den afbalancerede kemiske ligning:
ca (OH) ₂ (aq) + 2 hno₂ (aq) → Ca (no₂) ₂ (aq) + 2 h₂o (l)
Forklaring:
* Calciumhydroxid (CA (OH) ₂) er en stærk base. Det adskiller sig fuldstændigt i vand og frigiver hydroxidioner (OH⁻).
* nitrosyre (hno₂) er en svag syre. Det adskiller sig delvis i vand og frigiver hydrogenioner (H⁺).
* neutraliseringsreaktion: Hydroxidionerne fra basen reagerer med hydrogenionerne fra syren til dannelse af vand (H₂O).
* calciumnitrit (CA (no₂) ₂) er et opløseligt salt. Det opløses i vand og forbliver i opløsning.
Vigtige noter:
* Reaktionen er eksoterm, hvilket betyder, at den frigiver varme.
* Reaktionen udføres typisk i vandig opløsning.
* Nitrosyre er ustabil og nedbrydes let, så det er vigtigt at bruge friske opløsninger.
Denne reaktion er et klassisk eksempel på syre-base-kemi og demonstrerer de grundlæggende principper for neutraliseringsreaktioner.
 Varme artikler
Varme artikler
-
 Miljøvenligt tekstilmateriale er nemt og billigt at fremstilleMostafa Jabbari demonstrerer opløsningsmidlet, som påføres plyamidtekstilet. Kredit:Universitetet i Borås Da ph.d.-studerende Mostafa Jabbari begyndte sit forskningsprojekt, formålet var at forbed
Miljøvenligt tekstilmateriale er nemt og billigt at fremstilleMostafa Jabbari demonstrerer opløsningsmidlet, som påføres plyamidtekstilet. Kredit:Universitetet i Borås Da ph.d.-studerende Mostafa Jabbari begyndte sit forskningsprojekt, formålet var at forbed -
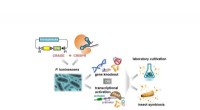 Udtrækning af hemmeligheder bag sekundære metabolitterVed at kombinere CRAGE- og CRISPR-teknologier har forskerne en meget nemmere metode til at karakterisere sekundære metabolitter. Kredit:Cell Chemical Biology (2021). DOI:10.1016/j.chembiol.2021.08.009
Udtrækning af hemmeligheder bag sekundære metabolitterVed at kombinere CRAGE- og CRISPR-teknologier har forskerne en meget nemmere metode til at karakterisere sekundære metabolitter. Kredit:Cell Chemical Biology (2021). DOI:10.1016/j.chembiol.2021.08.009 -
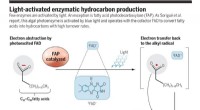 Et algenfotoenzym, der bruger blåt lys til at omdanne fedtsyrer til kulbrinterLysaktiveret enzymatisk kulbrinteproduktion. Kredit:(c) A. Kitterman / Videnskab , DOI:10.1126/science.aao4399 (Phys.org) - Et team af forskere tilknyttet flere institutioner i Frankrig har opda
Et algenfotoenzym, der bruger blåt lys til at omdanne fedtsyrer til kulbrinterLysaktiveret enzymatisk kulbrinteproduktion. Kredit:(c) A. Kitterman / Videnskab , DOI:10.1126/science.aao4399 (Phys.org) - Et team af forskere tilknyttet flere institutioner i Frankrig har opda -
 Holdbare træsvampe fungerer som grønne sensorer for mekanisk belastningPå dette fotografi, en træ carbon svamp genopretter til sin oprindelige form efter komprimering. Kredit:Chen et al. Slå den helt rigtige balance mellem blødhed og robusthed, balsatræ er et valgmat
Holdbare træsvampe fungerer som grønne sensorer for mekanisk belastningPå dette fotografi, en træ carbon svamp genopretter til sin oprindelige form efter komprimering. Kredit:Chen et al. Slå den helt rigtige balance mellem blødhed og robusthed, balsatræ er et valgmat
- Hvad er forholdet mellem volumen og tryk på en gas kaldet?
- At studere vampyrflagermus for at forudsige den næste pandemi
- Duellerende pickups, populær SUV blandt nye modeller, der kommer i 2018
- Hvilken type stødende sten har luftbobler i det?
- Hvad er de tre vandfaser?
- Hvor mange protoner neutroner og elektroner har tantal?


