Hvilken af de følgende to forbindelser har stærkeste nitrogen-nitrogenbinding H2NNH2 eller HNNH?
Forståelse af obligationsstyrke
* obligationsordre: Jo højere obligationsordren er, jo stærkere er bindingen. Obligationsordre er antallet af kemiske bindinger mellem to atomer.
* Elektrondensitet: Større elektrondensitet mellem de to atomer fører til en stærkere attraktion og dermed en stærkere binding.
analyse af forbindelserne
* h₂nnh₂ (hydrazin):
* Nitrogenatomerne i hydrazin er forbundet med en enkelt binding, hvilket giver en bindingsordre på 1.
* De ensomme par på nitrogenatomerne bidrager til en vis elektrondensitet mellem nitrogenatomerne.
* hnnh (diazomethane):
* Nitrogenatomerne i diazomethan er forbundet med en dobbeltbinding, hvilket giver en bindingsordre på 2.
* Dobbeltbindingen giver signifikant mere elektrondensitet mellem nitrogenatomerne.
Konklusion
Diazomethan (HNNH) har en stærkere nitrogen-nitrogenbinding, fordi det har en højere bindingsordre (dobbeltbinding) og større elektrondensitet mellem nitrogenatomerne.
 Varme artikler
Varme artikler
-
 Spinding af højstyrke polymer nanofibreRamesh Shrestha, Maarten de Boer, og Sheng Shen har transformeret polymerer fra bløde og termisk isolerende materialer til et ultra-stærkt og termisk ledende materiale. Kredit:College of Engineering,
Spinding af højstyrke polymer nanofibreRamesh Shrestha, Maarten de Boer, og Sheng Shen har transformeret polymerer fra bløde og termisk isolerende materialer til et ultra-stærkt og termisk ledende materiale. Kredit:College of Engineering, -
 Udvikling af ny fotovoltaisk kommercialiseringsteknologiProfessor Jongmin Choi, Institut for Energividenskab og Teknik, DGIST. Kredit:DGIST En teknologi til yderligere at fremskynde kommercialiseringen af Colloidal Quantum Dot (CQD) fotovoltaiske (PV
Udvikling af ny fotovoltaisk kommercialiseringsteknologiProfessor Jongmin Choi, Institut for Energividenskab og Teknik, DGIST. Kredit:DGIST En teknologi til yderligere at fremskynde kommercialiseringen af Colloidal Quantum Dot (CQD) fotovoltaiske (PV -
 Ingeniører gør injicerbare væv til en realitetDoktorand Mohamed Gamal bruger en nyudviklet celleindkapslingsanordning. Kredit:Nathan Skolski, UBC Okanagan En simpel injektion, der kan hjælpe med at genskabe beskadiget væv, har længe været drø
Ingeniører gør injicerbare væv til en realitetDoktorand Mohamed Gamal bruger en nyudviklet celleindkapslingsanordning. Kredit:Nathan Skolski, UBC Okanagan En simpel injektion, der kan hjælpe med at genskabe beskadiget væv, har længe været drø -
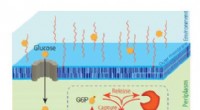 Opdagelse af nyt fænomen en game-changer for effektiv bioproduktion af nyttige kemikalierG6P-sekretionsmekanismen opdaget i denne undersøgelse. Kredit:Kobe University Et forskningssamarbejde har opdaget en ny mekanisme, hvorved glukose, der blev fanget af E. coli, derefter udskilles fr
Opdagelse af nyt fænomen en game-changer for effektiv bioproduktion af nyttige kemikalierG6P-sekretionsmekanismen opdaget i denne undersøgelse. Kredit:Kobe University Et forskningssamarbejde har opdaget en ny mekanisme, hvorved glukose, der blev fanget af E. coli, derefter udskilles fr
- Hvad vil der ske, hvis densiteten af kuglelejer er mindre end glycerololie?
- Et aktivt metal og halogen reagerer på dannelse af A?
- Hvorfor multipartite virus inficerer planter i stedet for dyr
- Tykke aflejringer af vindblæst finkornede sedimenter?
- Er hydrogenchlorid opløseligt eller uopløseligt i organiske opløsningsmidler?
- Hvilket af disse refererer til et lille stykke himmelrester, der har ramt overfladeplaneten?


