Hvor mange mol iltgas er nødvendige for at reagere med 10,0 mol ammoniak?
1. Skriv den afbalancerede kemiske ligning:
4 NH₃ (G) + 5 O₂ (G) → 4 Nej (G) + 6 H₂O (G)
2. Bestem molforholdet mellem ammoniak (NH₃) og ilt (O₂):
Den afbalancerede ligning viser, at 4 mol NH₃ reagerer med 5 mol O₂.
3. Beregn molen for iltbehov:
* Opret en andel: (5 mol o₂) / (4 mol nh₃) =(x mol o₂) / (10,0 mol nh₃)
* Løs for x: x =(5 mol o₂ * 10,0 mol nh₃) / 4 mol nh₃ =12,5 mol o₂
Derfor er der behov for 12,5 mol iltgas for at reagere med 10,0 mol ammoniak.
Sidste artikelHvad er atomnummeret n?
Næste artikelHvad er atomantallet af nitrat?
 Varme artikler
Varme artikler
-
 Tværfagligt team designer gasflowcelle til at analysere katalytisk adfærdMed hjælp fra andre forskere fra ORNL og Colorado State University, Daniel Olds og Katharine Page udviklede en gasstrømscelle med U-rør til at studere katalysatorer og bedre forstå, hvordan de letter
Tværfagligt team designer gasflowcelle til at analysere katalytisk adfærdMed hjælp fra andre forskere fra ORNL og Colorado State University, Daniel Olds og Katharine Page udviklede en gasstrømscelle med U-rør til at studere katalysatorer og bedre forstå, hvordan de letter -
 Smeltning af skrottede enheder, da bæredygtige behov opvarmesKredit:University of Queensland Smeltning af metaller fra kasserede elektroniske enheder er blandt løsninger til bæredygtig forsyning af kritiske materialer, der undersøges af forskere fra Univers
Smeltning af skrottede enheder, da bæredygtige behov opvarmesKredit:University of Queensland Smeltning af metaller fra kasserede elektroniske enheder er blandt løsninger til bæredygtig forsyning af kritiske materialer, der undersøges af forskere fra Univers -
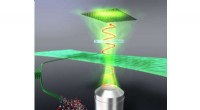 Fra nata de coco til computerskærme:Cellulose får en chance for at skinneKontrol af optisk retardering af den justerede cellulosefilm. Kredit:Osaka University Et hold ved Institute of Scientific and Industrial Research ved Osaka University har bestemt de optiske parame
Fra nata de coco til computerskærme:Cellulose får en chance for at skinneKontrol af optisk retardering af den justerede cellulosefilm. Kredit:Osaka University Et hold ved Institute of Scientific and Industrial Research ved Osaka University har bestemt de optiske parame -
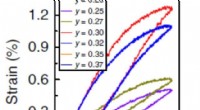 Nyt keramisk materiale kan reducere omkostningerne til piezoelektriske enhederKredit:Indian Institute of Science 1 procent), som er en markering af, hvor meget materialet kan ændre sin form, når det elektriske felt påføres. Imidlertid, de er meget dyre og svære at fremstill
Nyt keramisk materiale kan reducere omkostningerne til piezoelektriske enhederKredit:Indian Institute of Science 1 procent), som er en markering af, hvor meget materialet kan ændre sin form, når det elektriske felt påføres. Imidlertid, de er meget dyre og svære at fremstill
- Hvad er den oprindelige kilde til vindenergi?
- Theon-Kepler bifokalt teleskop hjælper med at fremme radialskærende interferometri
- Hvilken form for terrestial transport er den mindst effektive med hensyn til energiforbrug?
- Hvordan bruges vand i nuklear energi?
- Forskere udtænker en ny måde at undersøge bevægelsen af lavenergi-elektroner på
- Forskere graver i tilfælde af geologisk amnesi


