Er natriumoxid opløseligt i vand?
Her er hvorfor:
* ionisk forbindelse: Natriumoxid er en ionisk forbindelse, hvilket betyder, at det dannes af den elektrostatiske tiltrækning mellem positivt ladede natriumioner (Na+) og negativt ladede oxidioner (O²⁻).
* vandets polaritet: Vand (H₂O) er et polært molekyle, hvilket betyder, at det har en lidt positiv ende (brint) og en lidt negativ ende (ilt). Denne polaritet giver vand mulighed for at interagere stærkt med ioner.
* opløsning: Når natriumoxid tilsættes til vand, omgiver de polære vandmolekyler natrium- og oxidionerne, hvilket bryder de ioniske bindinger, der holder dem sammen i det faste stof. Ionerne bliver hydreret (omgivet af vandmolekyler) og spreder sig under hele opløsningen.
Reaktion med vand:
Opløsningen af natriumoxid i vand er en eksoterm reaktion, hvilket betyder, at den frigiver varme. Det danner en opløsning af natriumhydroxid (NaOH):
Na₂o (S) + H₂O (L) → 2 NaOH (AQ)
Vigtig note: Reaktionen mellem natriumoxid og vand er ret kraftig og producerer en masse varme. Det er vigtigt at håndtere natriumoxid med forsigtighed.
 Varme artikler
Varme artikler
-
 Lab-on-a-chip hjælper med at søge efter menneskeligt DNA på gerningsstederKredit:CC0 Public Domain Takket være det arbejde, der udføres af University of Twente Ph.D. kandidat Brigitte Bruijns, gerningssteder kan nu inspiceres på stedet for tilstedeværelsen af menneske
Lab-on-a-chip hjælper med at søge efter menneskeligt DNA på gerningsstederKredit:CC0 Public Domain Takket være det arbejde, der udføres af University of Twente Ph.D. kandidat Brigitte Bruijns, gerningssteder kan nu inspiceres på stedet for tilstedeværelsen af menneske -
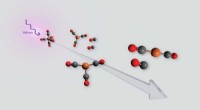 Ser lys bryde en model fotokatalysator ned i næsten realtidSkildring af den foreslåede mekanisme for nedbrydning af jernpentacarbonyl, når den udsættes for ultraviolet lys ved 199 nanometer bølgelængde. Kredit:Research Publishing International Ltd. Kemike
Ser lys bryde en model fotokatalysator ned i næsten realtidSkildring af den foreslåede mekanisme for nedbrydning af jernpentacarbonyl, når den udsættes for ultraviolet lys ved 199 nanometer bølgelængde. Kredit:Research Publishing International Ltd. Kemike -
 Elektronisk chip efterligner hjernen for at skabe minder på et øjeblikNy chip er baseret på et ultratyndt materiale, der ændrer elektrisk modstand som reaktion på forskellige bølgelængder af lys. Kredit:RMIT University Forskere fra RMIT University har hentet inspira
Elektronisk chip efterligner hjernen for at skabe minder på et øjeblikNy chip er baseret på et ultratyndt materiale, der ændrer elektrisk modstand som reaktion på forskellige bølgelængder af lys. Kredit:RMIT University Forskere fra RMIT University har hentet inspira -
 Ny effektiv katalysator til nøgletrin i kunstig fotosynteseForskningsteamets leder Javier Concepcion (stående, venstre) med Yan Xie, David Shaffer, og David Szalda. Kredit:Brookhaven National Laboratory Kemikere ved det amerikanske energiministeriums Broo
Ny effektiv katalysator til nøgletrin i kunstig fotosynteseForskningsteamets leder Javier Concepcion (stående, venstre) med Yan Xie, David Shaffer, og David Szalda. Kredit:Brookhaven National Laboratory Kemikere ved det amerikanske energiministeriums Broo
- Hvilken bane er der stadig i den yderste del af atmosfæren?
- En ny tilgang til at opnå stabilitet, laserpulser med høj repetitionshastighed
- Hvor dannes kemiske bjergarter?
- Fysikere observerer længe søgt fænomen i nanoskala
- Brand regnbuer og solhunde:Underligt vejr i smartphonealderen
- Vil fødekæderne bryde, efterhånden som sæsonerne bliver mere uforudsigelige?


