Hvem har den stærkere dipol-dipolhydrogenchlorid eller melid?
Her er hvorfor:
* Elektronegativitetsforskel: Fluor er meget mere elektronegativ end klor. Dette betyder, at fluoratomet i HF trækker de delte elektroner meget stærkere over for sig selv, hvilket skaber en større delvis negativ ladning på fluoren og en større delvis positiv ladning på brintet. Dette resulterer i et stærkere dipolmoment i HF.
* mindre størrelse af fluor: Fluor er mindre end klor, hvilket fører til en mere koncentreret delvis negativ ladning på fluoratomet. Dette forbedrer yderligere dipol-dipolinteraktionerne i HF.
Kortfattet: Den større elektronegativitetsforskel og mindre størrelse af fluor i HF bidrager til stærkere dipol-dipolinteraktioner sammenlignet med HCI.
 Varme artikler
Varme artikler
-
 Et kræftkværnemiddel med ny virkningsmekanisme fundetAt bekæmpe kræft med et nyudviklet stof, der nedbryder kræftfremkaldende nordlysproteiner:Dette er målet for en ny undersøgelse foretaget af forskere ved universiteter i Würzburg og Frankfurt. Kredit:
Et kræftkværnemiddel med ny virkningsmekanisme fundetAt bekæmpe kræft med et nyudviklet stof, der nedbryder kræftfremkaldende nordlysproteiner:Dette er målet for en ny undersøgelse foretaget af forskere ved universiteter i Würzburg og Frankfurt. Kredit: -
 3D-print af stivelse til personlig udvikling af medicin3D-print gør det muligt at fremstille personaliserede lægemidler skræddersyet til den enkelte patient. Kredit:UPV/EHU Traditionelle metoder producerer lægemidler med specifikke parametre, men i man
3D-print af stivelse til personlig udvikling af medicin3D-print gør det muligt at fremstille personaliserede lægemidler skræddersyet til den enkelte patient. Kredit:UPV/EHU Traditionelle metoder producerer lægemidler med specifikke parametre, men i man -
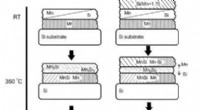 Fysikere overvåger dannelsen af film med højere mangansilicidSkematisk illustration af synteseproceduren til venstre:Mn17Si30 og højre Mn4Si7 -prøve. Kredit:Ivan Tarasov Et team fra Kirensky Institute of Physics (Siberian Branch of the Russian Academy of Sc
Fysikere overvåger dannelsen af film med højere mangansilicidSkematisk illustration af synteseproceduren til venstre:Mn17Si30 og højre Mn4Si7 -prøve. Kredit:Ivan Tarasov Et team fra Kirensky Institute of Physics (Siberian Branch of the Russian Academy of Sc -
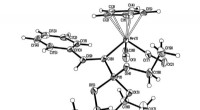 Kemikere opdager en ny dannelsesmekanisme for kræftbekæmpende stofferEt af cymantrenderivaterne, der blev brugt i undersøgelsen. Kredit:Alexander Smolyakov RUDN Universitets kemikere reviderede dannelsesmekanismen for organofosforkomplekser med metal. Resultaterne
Kemikere opdager en ny dannelsesmekanisme for kræftbekæmpende stofferEt af cymantrenderivaterne, der blev brugt i undersøgelsen. Kredit:Alexander Smolyakov RUDN Universitets kemikere reviderede dannelsesmekanismen for organofosforkomplekser med metal. Resultaterne
- Hvad er fysikbegrebet langsomt glas?
- At bryde igennem grænserne for en enkelt fiber laserforstærker:Kohærent strålekombination
- Hvad vil der ske, hvis du bruger mindre elektricitet?
- Metastabile metalliske nanopartikler kan finde anvendelse i elektronik, optik
- Hvordan vil du beskrive rækkefølgen af oxygencarbondioxid og blod ud fra dine egne ord?
- Brug af chirale guld-nanopartikler til at forbedre immunrespons


