Hvorfor kan kun fire atomer af fosfor producere to molekyler diphosphor -trioxid, selv når der er et overskydende iltatomer?
Her er hvorfor:
* støkiometri: Den afbalancerede kemiske ligning for reaktionen mellem fosfor og ilt til dannelse af diphosphor -trioxid er:
4 P + 3 O₂ → 2 P₂O₃
* Ligningen forklarer det hele: Denne ligning viser, at 4 mol phosphor (P) reagerer med 3 mol ilt (O₂) for at producere 2 mol diphosphor -trioxid (P₂O₃).
* overskydende ilt ændrer ikke forholdet: Selv hvis du har et overskud af ilt, vil reaktionen stadig kun forbruge 3 mol O₂ for hver 4 mol af P. Det overskydende ilt forbliver ikke -reageret.
Kort sagt: Mens overskydende ilt er til stede, ændrer det ikke det grundlæggende forhold mellem reaktanter og produkter dikteret af den afbalancerede kemiske ligning. Reaktionen vil stadig producere 2 mol diphosphor -trioxid for hver 4 mol af det anvendte fosfor, uanset hvilken mængde ilt der er tilgængeligt.
Sidste artikelHvor mange atomer i trinitrotoluen?
Næste artikelHvad er den nettoioniske ligning af na oh-h cl-h2o cl?
 Varme artikler
Varme artikler
-
 Diamant i nanostørrelse vil forbedre materialer til søtransportNikolai Kakhidze, en kandidatstuderende ved Det Fysiske og Tekniske Fakultet, som netop er vendt tilbage fra praktik på Brunel University Et eksperiment på introduktionen af nanoskala diamant i
Diamant i nanostørrelse vil forbedre materialer til søtransportNikolai Kakhidze, en kandidatstuderende ved Det Fysiske og Tekniske Fakultet, som netop er vendt tilbage fra praktik på Brunel University Et eksperiment på introduktionen af nanoskala diamant i -
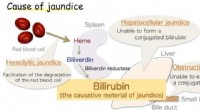 Forskere får gennembrud i antioxidantenzym forbundet med gulsotFig.1:Årsag til gulsot. Bilirubin er det forårsagende materiale til gulsot. Kredit:Osaka University Et japansk forskerhold involveret Osaka University undersøgte biliverdin reduktase, enzymet, der
Forskere får gennembrud i antioxidantenzym forbundet med gulsotFig.1:Årsag til gulsot. Bilirubin er det forårsagende materiale til gulsot. Kredit:Osaka University Et japansk forskerhold involveret Osaka University undersøgte biliverdin reduktase, enzymet, der -
 Genbrug af plastik:Vinylpolymer nedbrudt til aspirinkomponenterDer går ikke en dag uden nyheder om mikroplastik i vores have. Der er ikke mange effektive metoder til genanvendelse af plast uden at gå på kompromis med kvaliteten. Et fyrtårn af håb blev for nylig t
Genbrug af plastik:Vinylpolymer nedbrudt til aspirinkomponenterDer går ikke en dag uden nyheder om mikroplastik i vores have. Der er ikke mange effektive metoder til genanvendelse af plast uden at gå på kompromis med kvaliteten. Et fyrtårn af håb blev for nylig t -
 Inosin kan være en potentiel vej til det første RNA og livets oprindelse på JordenEt sted i det fjendtlige miljø på den tidlige Jord, livet blev født. Kredit:Harvard University Vores forhistoriske jord, bombarderet med asteroider og lyn, fyldt med boblende geotermiske pools, vi
Inosin kan være en potentiel vej til det første RNA og livets oprindelse på JordenEt sted i det fjendtlige miljø på den tidlige Jord, livet blev født. Kredit:Harvard University Vores forhistoriske jord, bombarderet med asteroider og lyn, fyldt med boblende geotermiske pools, vi
- Forskere udvikler en ny type optisk fiber, der bevarer lysets egenskaber
- Hvad er de videnskabelige klassifikationer af svampe?
- Ny forskning afslører, hvorfor fiskere fortsætter med at fiske på trods af svindende fangster
- Ny teori lover at omforme, hvordan vi tænker om polymeroverbygninger
- Californiens værste naturbrande hjælper med at forbedre forudsigelsen af luftkvaliteten
- Hvad er et eksempel på energioverførsel ved stråling?


