Skriv reaktionerne fra natriumperoxid med vand?
Reaktionsligning:
2 Na₂o₂ + 2 H₂O → 4 NaOH + H₂O₂
Forklaring:
* Natriumperoxid (Na₂o₂) er et stærkt oxidationsmiddel, og vand (H₂O) fungerer som et reducerende middel.
* Reaktionen frigiver varme, hvilket får opløsningen til at blive varm.
* Hydrogenperoxid (H₂O₂) dannet er et kraftfuldt oxidationsmiddel og kan yderligere reagere med natriumhydroxid (NaOH).
* Reaktionen producerer også iltgas (O₂), som kan observeres som bobler.
Generelt er reaktionen af natriumperoxid med vand en kompleks proces, der involverer flere trin og producerer flere produkter.
Sikkerhedsforholdsregler:
* Natriumperoxid er et stærkt oxidationsmiddel og bør håndteres med omhu.
* Undgå kontakt med hud, øjne og tøj.
* Brug passende sikkerhedsudstyr, inklusive handsker, beskyttelsesbriller og en laboratoriefrakke.
* Opbevar natriumperoxid i et køligt, tørt sted væk fra brændbare materialer.
* Bland ikke natriumperoxid med syrer eller andre oxidationsmidler.
Bemærk: Reaktionen af natriumperoxid med vand kan være farlig, hvis den ikke håndteres korrekt. Det er vigtigt at tage de nødvendige forholdsregler og konsultere en kvalificeret kemiker for vejledning.
Sidste artikelHvad er fasen af zirconium ved STP?
Næste artikelHvad kaldes brint og ilt?
 Varme artikler
Varme artikler
-
 Video:Kemikalierne, vi efterladerKredit:The American Chemical Society Alt, hvad vi bruger, er lavet af kemikalier. Så det er ikke overraskende, at vi opfanger en masse fremmede molekyler fra det, vi støder ind i hele tiden, fra v
Video:Kemikalierne, vi efterladerKredit:The American Chemical Society Alt, hvad vi bruger, er lavet af kemikalier. Så det er ikke overraskende, at vi opfanger en masse fremmede molekyler fra det, vi støder ind i hele tiden, fra v -
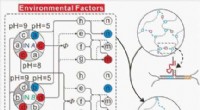 Ændring af blødt stofs form ved hjælp af logiske kredsløb lavet af DNAKredit: Angewandte Chemie International Edition (2021). DOI:10.1002/anie.202102169 De utallige processer, der foregår i biologiske celler, kan ved første øjekast virke utroligt komplekse. Og stad
Ændring af blødt stofs form ved hjælp af logiske kredsløb lavet af DNAKredit: Angewandte Chemie International Edition (2021). DOI:10.1002/anie.202102169 De utallige processer, der foregår i biologiske celler, kan ved første øjekast virke utroligt komplekse. Og stad -
 Kemiker skaber næste generation af neurovidenskabelige værktøjerRobert Campbell, professor i kemi, bygger nye værktøjer til neuroforskere i sit laboratorium på University of Alberta. Kredit:University of Alberta UAlberta kemiprofessor Robert Campbell udvikler
Kemiker skaber næste generation af neurovidenskabelige værktøjerRobert Campbell, professor i kemi, bygger nye værktøjer til neuroforskere i sit laboratorium på University of Alberta. Kredit:University of Alberta UAlberta kemiprofessor Robert Campbell udvikler -
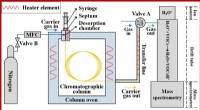 Butanol i latexmaling detekteret ved massespektrometriteknologiSkematisk diagram af FastGC-PTR-MS. Kredit:Sun Qin Ifølge en undersøgelse offentliggjort i Journal of Chromatography A , ved hjælp af hurtig gaskromatografi protonoverførsel reaktion massespektrome
Butanol i latexmaling detekteret ved massespektrometriteknologiSkematisk diagram af FastGC-PTR-MS. Kredit:Sun Qin Ifølge en undersøgelse offentliggjort i Journal of Chromatography A , ved hjælp af hurtig gaskromatografi protonoverførsel reaktion massespektrome
- Hvor er Apollo 11 Lunar Ascent -modul nu stadig kredivt månen eller styrtede ned?
- Whirlpools på nanoskalaen kan formere magnetisk hukommelse
- Et stof, der er opløst i vand, er betegnet?
- Fysikers arbejde kan hjælpe med at ændre transistors fremtid
- Hvad er så unikt ved troperne? 'Mindre end vi troede'
- Forskelle i wolframisotoper viser, at jordens overflade er dannet ujævnt


