Hvad er produktet af konvertering ammoniak til et mindre giftigt stof?
1. Oxidation til nitrogen:
* reaktion: 4 NH3 + 3 O2 → 2 N2 + 6 H2O
* Forklaring: Ammoniak kan oxideres i nærvær af en katalysator som platin eller et metaloxid til dannelse af nitrogengas (N2) og vand (H2O). Nitrogen er en ufarlig gas, der udgør størstedelen af vores atmosfære.
2. Reaktion med syre:
* reaktion: NH3 + HCL → NH4CL
* Forklaring: Ammoniak reagerer let med syrer som saltsyre (HCI) for at danne ammoniumchlorid (NH4CL). Ammoniumchlorid er et fast salt, langt mindre flygtigt end ammoniak og betragtes generelt som mindre giftigt.
3. Absorption i vand:
* reaktion: NH3 + H2O ⇌ NH4 + + OH-
* Forklaring: Ammoniak opløses i vand og danner ammoniumioner (NH4+) og hydroxidioner (OH-). Tilstedeværelsen af disse ioner ændrer pH -værdien i opløsningen, men producerer ikke direkte et mindre giftigt stof. Ammoniumionerne er imidlertid mindre ustabile og mindre irriterende end ammoniakgas.
4. Biologiske processer:
* nitrifikation: Mikroorganismer i jord kan omdanne ammoniak til nitrit (NO2-) og derefter nitrat (NO3-). Disse former er mindre giftige end ammoniak og kan bruges af planter som næringsstoffer.
Den mest passende metode til omdannelse af ammoniak til et mindre giftigt stof afhænger af den specifikke kontekst og det ønskede resultat. I spildevandsrensning bruges for eksempel ofte biologisk nitrifikation, mens industrielle processer muligvis bruger oxidation til nitrogen.
Det er vigtigt at bemærke, at selvom produkterne fra ammoniakkonvertering generelt betragtes som mindre giftige, kan de stadig udgøre miljørisici eller sundhedsfarer afhængigt af deres koncentration og den specifikke anvendelse.
Sidste artikelVandig saltsyre plus vandigt bariumhydroxid giver chloridvand?
Næste artikelHvad er virkningen af temperatur på PH af vand?
 Varme artikler
Varme artikler
-
 Ny sensor registrerer værdifuldt sjældent jordelement terbium fra utraditionelle kilderProteinet lanmodulin er blevet udviklet til en sensor til at identificere det sjældne jordelement terbium fra komplekse miljøer, såsom syredrainafvanding. Sensoren, illustreret her, udsender grønt lys
Ny sensor registrerer værdifuldt sjældent jordelement terbium fra utraditionelle kilderProteinet lanmodulin er blevet udviklet til en sensor til at identificere det sjældne jordelement terbium fra komplekse miljøer, såsom syredrainafvanding. Sensoren, illustreret her, udsender grønt lys -
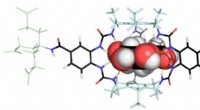 Glucosebindende molekyle kunne transformere behandlingen af diabetesReceptor bindende glucose. Kredit:University of Bristol Forskere fra University of Bristol har designet en ny syntetisk glukosebindende molekyleplatform, der bringer os et skridt tættere på udvikl
Glucosebindende molekyle kunne transformere behandlingen af diabetesReceptor bindende glucose. Kredit:University of Bristol Forskere fra University of Bristol har designet en ny syntetisk glukosebindende molekyleplatform, der bringer os et skridt tættere på udvikl -
 DNA -enzymer kunne udkonkurrere proteinenzymer til genteknologiKemiprofessor Yi Lu ledede et team, der udviklede en teknik, der tillader DNA-enzymer at skære dobbeltstrenget DNA, muliggøre en bred vifte af gentekniske applikationer. Kredit:L. Brian Stauffer F
DNA -enzymer kunne udkonkurrere proteinenzymer til genteknologiKemiprofessor Yi Lu ledede et team, der udviklede en teknik, der tillader DNA-enzymer at skære dobbeltstrenget DNA, muliggøre en bred vifte af gentekniske applikationer. Kredit:L. Brian Stauffer F -
 Video:Hvordan hårfarve virkerKredit:The American Chemical Society Uanset om du har brug for en forklædning for at løbe fra loven eller bare prøver at efterligne *NSYNC-tidens frostede tip, du kan få brug for noget kemisk assi
Video:Hvordan hårfarve virkerKredit:The American Chemical Society Uanset om du har brug for en forklædning for at løbe fra loven eller bare prøver at efterligne *NSYNC-tidens frostede tip, du kan få brug for noget kemisk assi
- Hvad er energitransformation, når du klatrer op ad trappen?
- Hvorfor tror du, at Linnaeus ikke omfattede klassificeringskongeriger for kategorier af archaea og b…
- I fornyelse, Facebook satser på mindre forbindelser, romantik
- Apple fortæller medarbejderne, hvorfor det ikke hjælper med at hacke skydespillerens telefon (Opda…
- Hvilken type bakterier lever af døde ting?
- Fugleinfluenza uhyggeligt spørgsmål:hvordan dræber man millioner af fjerkræ


