Hvad er den molekylære form af svovltrioxid?
Her er hvorfor:
* Centralatom: Svovl (er) er det centrale atom.
* Valenselektroner: Svovl har 6 valenselektroner, og hvert ilt (O) atom har 6 valenselektroner.
* binding: Svovl danner dobbeltbindinger med hvert af de tre iltatomer.
* Elektronpar: Der er tre bindingspar og ingen ensomme par på svovlatomet.
* form: I henhold til VSEPR -teori (Valence Shell Electron Pair Repulsion) vil elektronparre arrangere sig selv til at minimere frastødning, hvilket fører til en trigonal plan geometri med bindingsvinkler på 120 grader.
Sidste artikelHvad er den kemiske formel for jernholdigt disulfid?
Næste artikelHvad er den molekylære iltformel?
 Varme artikler
Varme artikler
-
 Katalysatorer for bedre produktion af biobrændstofKredit:Teguh Jati Prasetyo, Shutterstock Biomasse er langt mere kompleks end konventionelt råmateriale, og udviklingen af de nødvendige katalysatorer er traditionelt en langvarig og kompliceret
Katalysatorer for bedre produktion af biobrændstofKredit:Teguh Jati Prasetyo, Shutterstock Biomasse er langt mere kompleks end konventionelt råmateriale, og udviklingen af de nødvendige katalysatorer er traditionelt en langvarig og kompliceret -
 Neutrondiffraktionsforsøg af materialer med strukturer bestående af flere metalelementerKredit:Institut Laue-Langevin Materialer, der indeholder flere metalelementer, er vigtige til forskellige anvendelser, da kombinationen af forskellige metalkationer giver nye eller forbedrede eg
Neutrondiffraktionsforsøg af materialer med strukturer bestående af flere metalelementerKredit:Institut Laue-Langevin Materialer, der indeholder flere metalelementer, er vigtige til forskellige anvendelser, da kombinationen af forskellige metalkationer giver nye eller forbedrede eg -
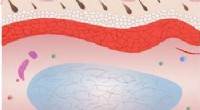 Hydrogel heler uden tilsætningsstofferEn illustration viser, hvordan over seks uger, fra top til bund, en hydrogel, der er udviklet ved Rice University, hjælper med vævsremodellering. Processen begynder med celleinfiltration efterfulgt af
Hydrogel heler uden tilsætningsstofferEn illustration viser, hvordan over seks uger, fra top til bund, en hydrogel, der er udviklet ved Rice University, hjælper med vævsremodellering. Processen begynder med celleinfiltration efterfulgt af -
 Puster nyt liv i eksisterende teknologi:FT-IR-spektrometer viser molekylær orientering3D-printbar optisk opsætning med indbygget prøvekammer til et FT-IR-spektrometer. Prøven sættes på Si ATR-krystallerne til måling. Kredit:©M. Takahashi &K. Okada, Osaka Prefecture University Forsk
Puster nyt liv i eksisterende teknologi:FT-IR-spektrometer viser molekylær orientering3D-printbar optisk opsætning med indbygget prøvekammer til et FT-IR-spektrometer. Prøven sættes på Si ATR-krystallerne til måling. Kredit:©M. Takahashi &K. Okada, Osaka Prefecture University Forsk


