Handling af varme på sølvnitrat?
1. Blid opvarmning:
* nedenfor smeltepunkt (~ 212 ° C): Når det opvarmes forsigtigt, smelter sølvnitraten uden nedbrydning. Det bliver en væske, men dens kemiske sammensætning forbliver uændret.
2. Stærk opvarmning:
* Nedbrydning: Når der opvarmes stærkt, nedbrydes sølvnitrat til sølvmetal, nitrogendioxidgas og iltgas. Reaktionen fortsætter som følger:
`` `
2 AGNO₃ (S) → 2 AG (S) + 2 NO₂ (G) + O₂ (G)
`` `
Observationer:
* farveændring: Oprindeligt er sølvnitrat et hvidt fast stof. Ved opvarmning smelter det til en farveløs væske. Efterhånden som nedbrydningen skrider frem, bliver væsken sort på grund af dannelsen af sølvmetal.
* Gasudvikling: Du vil observere rødbrune dampe af nitrogendioxid (NO₂) undslippe. Gassen har en skarp lugt.
Vigtige noter:
* sikkerhed: Denne reaktion skal udføres i et godt ventileret område, da kvælstofdioxid er en giftig gas.
* tilstedeværelse af organisk stof: Hvis der er organisk stof (som sukker eller papir) til stede, kan nedbrydningen være mere kraftig, hvilket fører til sorte af det organiske materiale og dannelsen af sølvmetal. Dette er grundlaget for nogle fotografiske processer.
Ansøgninger:
* sølvproduktion: Nedbrydningen af sølvnitrat bruges til produktion af rent sølv.
* Fotografering: Tidligere var sølvnitrat en nøglekomponent i fotografiske processer, hvor det blev brugt til at skabe lysfølsomme sølvhalogenidkrystaller.
Fortæl mig, hvis du gerne vil undersøge ethvert specifikt aspekt af denne reaktion yderligere!
Sidste artikelHvorfor har natriumchlorid et smeltepunkt på 800?
Næste artikelKviksølvoxid opvarmes til dannelse af ilt?
 Varme artikler
Varme artikler
-
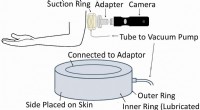 Ny enhed kan hjælpe med at minimere ardannelse ved kosmetisk kirurgiSkematisk af den nye enhed, der kan fastslå orienteringen af hudspændingslinjer. Kredit:Guy German Forskere ved Binghamton University, State University of New York har udviklet en ny enhed, der
Ny enhed kan hjælpe med at minimere ardannelse ved kosmetisk kirurgiSkematisk af den nye enhed, der kan fastslå orienteringen af hudspændingslinjer. Kredit:Guy German Forskere ved Binghamton University, State University of New York har udviklet en ny enhed, der -
 Verdens hastighedsrekord for polymersimuleringer knust med over hundrede gangeDr. Airidas Korolkovas er postdoktor ved Institut for Fysik og Astronomi, Uppsala Universitet, Sverige, og en langvarig gæst på Institut Laue-Langevin, 71 avenue des Martyrs, Grenoble, Frankrig. Kredi
Verdens hastighedsrekord for polymersimuleringer knust med over hundrede gangeDr. Airidas Korolkovas er postdoktor ved Institut for Fysik og Astronomi, Uppsala Universitet, Sverige, og en langvarig gæst på Institut Laue-Langevin, 71 avenue des Martyrs, Grenoble, Frankrig. Kredi -
 Video:Petrichor, lugten af regnKredit:The American Chemical Society Duften, der ledsager en forårsbyge, er så stemningsfuld, at den har sit eget ord:petrichor. Se, mens Reactions udforsker den unikke kemi bag lugten af regn:
Video:Petrichor, lugten af regnKredit:The American Chemical Society Duften, der ledsager en forårsbyge, er så stemningsfuld, at den har sit eget ord:petrichor. Se, mens Reactions udforsker den unikke kemi bag lugten af regn: -
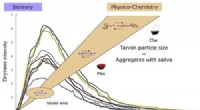 Hvorfor nogle rødvine smager tørtKredit:American Chemical Society Vinkendere kan nemt skelne mellem en tør rødvin, såsom Cabernet Sauvignon, fra en mere frugtbar rød, ligesom Pinot Noir. Forskere har længe forbundet følelsen af
Hvorfor nogle rødvine smager tørtKredit:American Chemical Society Vinkendere kan nemt skelne mellem en tør rødvin, såsom Cabernet Sauvignon, fra en mere frugtbar rød, ligesom Pinot Noir. Forskere har længe forbundet følelsen af


