Hvor mange flere elektroner har et atom af carbon behov for at afslutte sin valensskal?
Her er hvorfor:
* Carbon's atomstruktur: Carbon har 6 elektroner. Dens elektronkonfiguration er 2, 4. Dette betyder, at den har 2 elektroner i sin første skal og 4 elektroner i sin anden skal.
* Valence Shell: Den yderste skal af et atom kaldes valensskallen. For kulstof er valensskallen den anden skal.
* octet regel: Atomer har en tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration med 8 elektroner i deres valensskal (undtagen for brint og helium, som kun har brug for 2).
* Carbon's behov: Carbon har 4 elektroner i sin valensskal. For at opnå en stabil octet har den brug for 4 flere elektroner.
Dette er grunden til, at kulstof danner fire kovalente bindinger (deling af elektroner) med andre atomer, som i methan (CH4) eller kuldioxid (CO2).
Sidste artikelHvad er de tre måder, hvorpå et stof kan navngives?
Næste artikelHvad er den molekylære formel af sød og lav?
 Varme artikler
Varme artikler
-
 Bakterielle enzymer kapret til at skabe komplekse molekyler, der normalt fremstilles af planterKredit:CC0 Public Domain Kemikere ved Scripps Research har effektivt skabt tre familier af komplekse, oxygenholdige molekyler, der normalt kun kan opnås fra planter. Disse molekyler, kaldet terpe
Bakterielle enzymer kapret til at skabe komplekse molekyler, der normalt fremstilles af planterKredit:CC0 Public Domain Kemikere ved Scripps Research har effektivt skabt tre familier af komplekse, oxygenholdige molekyler, der normalt kun kan opnås fra planter. Disse molekyler, kaldet terpe -
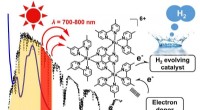 NIR-drevet H2-udvikling fra vand:Udvidet bølgelængdeområde for konvertering af solenergiNær-infrarødt-lysdrevet hydrogenudvikling fra vand fotodrevet af triruthenium fotosensibilisator. Kredit:Kyushu University Hydrogengas er et lovende grønt brændstof. Det letteste kemiske element,
NIR-drevet H2-udvikling fra vand:Udvidet bølgelængdeområde for konvertering af solenergiNær-infrarødt-lysdrevet hydrogenudvikling fra vand fotodrevet af triruthenium fotosensibilisator. Kredit:Kyushu University Hydrogengas er et lovende grønt brændstof. Det letteste kemiske element, -
 Nyt design af bioaktive peptidnanofibre, der holder både temperaturreversibilitet og stivhedskontro…Temperaturrespons af peptidet. Det danner fast (gel) ved 20 grader Celsius og flydende (sol) ved 80 grader Celsius angivet med hvide parenteser, og denne funktion er reversibel. Kredit:Takahiro Muraok
Nyt design af bioaktive peptidnanofibre, der holder både temperaturreversibilitet og stivhedskontro…Temperaturrespons af peptidet. Det danner fast (gel) ved 20 grader Celsius og flydende (sol) ved 80 grader Celsius angivet med hvide parenteser, og denne funktion er reversibel. Kredit:Takahiro Muraok -
 Materialeinformatik afslører ny klasse af superhårde legeringerEt røntgenenergi-dispersiv spektroskopi (EDS) kort over den støbte mikrostruktur af en hård legering forudsagt fra Lehigh University forskeres analyse. Bogstaver er røntgenintensitetskort forbundet me
Materialeinformatik afslører ny klasse af superhårde legeringerEt røntgenenergi-dispersiv spektroskopi (EDS) kort over den støbte mikrostruktur af en hård legering forudsagt fra Lehigh University forskeres analyse. Bogstaver er røntgenintensitetskort forbundet me


