Er forbindelser tilfældige kombinationer af elementer?
Her er hvorfor:
* Kemiske bindinger: Forbindelser dannes, når atomer af forskellige elementer binder sig sammen gennem specifikke kræfter kaldet kemiske bindinger. Disse bindinger kan være ioniske (overførsel af elektroner) eller kovalente (deling af elektroner). Den dannede bindingstype afhænger af de involverede elementer og deres elektronegativitet (tendens til at tiltrække elektroner).
* faste forhold: I en forbindelse er elementerne altid til stede i et fast forhold. Dette forhold bestemmes af den kemiske formel for forbindelsen og repræsenterer det enkleste hele antal forhold mellem atomer i forbindelsen. For eksempel har vand (H₂O) altid to hydrogenatomer for hvert iltatom.
* Unikke egenskaber: Forbindelser har unikke egenskaber, der adskiller sig fra egenskaberne for de elementer, der udgør dem. For eksempel er vand (H₂O) en væske ved stuetemperatur, mens brint (H₂) og ilt (O₂) er gasser.
Derfor er dannelsen af forbindelser ikke en tilfældig proces, men snarere en veldefineret kemisk proces, der følger specifikke regler og principper.
Sidste artikelEr CH3CH2CH2CH2CH3 og CH3CH2CH2CH2CH2CH3 blandbar CBR4 H20 Cl2 blandbar?
Næste artikelHvad er krystalformen af fluorit?
 Varme artikler
Varme artikler
-
 Ultrahurtige metalionbatterier baseret på nyt organisk katodemateriale er blevet udvikletKredit:CC0 Public Domain Forskere fra Skoltech Center for Energy Science and Technology, IPCP RAS og D.I. Mendeleev University of Chemical Technology har designet et nyt polymerkatodemateriale til
Ultrahurtige metalionbatterier baseret på nyt organisk katodemateriale er blevet udvikletKredit:CC0 Public Domain Forskere fra Skoltech Center for Energy Science and Technology, IPCP RAS og D.I. Mendeleev University of Chemical Technology har designet et nyt polymerkatodemateriale til -
 Kobberstearat lovende til tung olieoxidation, siger undersøgelseKredit:Kazan Federal University Kobbersalte har fundet plads i mange industrier fra lægemidler til landbrug, men de ses sjældent i petrokemi og olieudvinding. Nu, Forskere fra Kazan Federal Univer
Kobberstearat lovende til tung olieoxidation, siger undersøgelseKredit:Kazan Federal University Kobbersalte har fundet plads i mange industrier fra lægemidler til landbrug, men de ses sjældent i petrokemi og olieudvinding. Nu, Forskere fra Kazan Federal Univer -
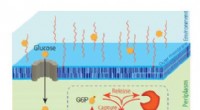 Opdagelse af nyt fænomen en game-changer for effektiv bioproduktion af nyttige kemikalierG6P-sekretionsmekanismen opdaget i denne undersøgelse. Kredit:Kobe University Et forskningssamarbejde har opdaget en ny mekanisme, hvorved glukose, der blev fanget af E. coli, derefter udskilles fr
Opdagelse af nyt fænomen en game-changer for effektiv bioproduktion af nyttige kemikalierG6P-sekretionsmekanismen opdaget i denne undersøgelse. Kredit:Kobe University Et forskningssamarbejde har opdaget en ny mekanisme, hvorved glukose, der blev fanget af E. coli, derefter udskilles fr -
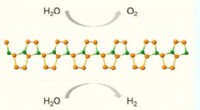 Tid til en ny konkurrent inden for energiomdannelse og lagringKAUST-teamet brugte state-of-the-art evolutionær søgning og beregninger af første principper til at forudsige strukturen af B 2 P 6 . Kredit:KAUST Evolutionær søgning har hjulpet forskere me
Tid til en ny konkurrent inden for energiomdannelse og lagringKAUST-teamet brugte state-of-the-art evolutionær søgning og beregninger af første principper til at forudsige strukturen af B 2 P 6 . Kredit:KAUST Evolutionær søgning har hjulpet forskere me
- Hvilken videnskabsmand opdagede, at elektroner flyttede i skaller?
- Solcelle udelukkende i kulstof udnytter infrarødt lys
- 3D-computermodellering simulerer påvirkninger, viser det mest effektive arrangement for tidevandsmø…
- Hvordan påvirker kinetisk energi stopafstanden på et køretøj?
- Uddybende spørgsmål:Hjælper det dem med at vokse at tale med planter?
- <p> Unge piger kan lide at lege i makeup, men det gør også voksne. Faktisk hjælper forskere med a…


