Er CH3CH2CH2CH2CH3 og CH3CH2CH2CH2CH2CH3 blandbar CBR4 H20 Cl2 blandbar?
Forståelse af blandbarhed
Lykbarhed henviser til to væskers evne til at blande og danne en homogen opløsning. Dette bestemmes stort set af polariteten af de involverede molekyler:
* polære molekyler: Har ujævn fordeling af elektroner, hvilket fører til delvis positive og negative afgifter. De har en tendens til at opløses i andre polære opløsningsmidler.
* ikke -polære molekyler: Har endda distribution af elektroner og ingen signifikante delvise afgifter. De har en tendens til at opløses i andre ikke -polære opløsningsmidler.
analyse af stofferne
1. Begge er alkaner, som er kulbrinter med kun enkeltbindinger. Dette gør dem ikke -polære. Da de begge er ikke -polære, er de blandbare .
2. CBR4 (carbon tetrabromid): Mens kulstof har en lidt højere elektronegativitet end brom, annullerer den tetrahedrale form af CBR4 dipolmomenterne. Dette gør det ikke -polært .
3. H2O (vand): På grund af forskellen i elektronegativitet mellem brint og ilt er vandmolekyler meget polære.
4. cl2 (klor): Chlor er et diatomisk molekyle med en ikke -polær kovalent binding. Det er ikke -polær .
Bestemmelse af blandbarhed
* pentan/hexan og CBR4: Alle tre er ikke -polære, så de vil være blandbare .
* pentan/hexan og H2O: Disse er henholdsvis ikke -polære og polære. "Som opløser som", hvilket betyder, at de vil være ublandbart (vil ikke blandes).
* CBR4 og H2O: Igen, ikke -polær og polær, hvilket gør dem ikke blandbare .
* CL2 og H2O: Ikke -polær og polær, hvilket fører til ublandbilitet .
Sammendrag:
* CH3CH2CH2CH2CH3 og CH3CH2CH2CH2CH2CH3 er blandbare med CBR4.
* Alle andre kombinationer er ikke -blandbare.
Sidste artikelHvilket element i en forbindelse vises først navnet?
Næste artikelEr forbindelser tilfældige kombinationer af elementer?
 Varme artikler
Varme artikler
-
 Ny solid-state termisk diode udviklet med bedre ensretterydelse(a) og (b) repræsenterer for den skematiske geometri af den termiske diode bestående af Ni0.85Fe0.15S og Al2O3 for fremadgående og tilbagegående retning. (c) Termisk ensretningsfaktor (γ) som funktion
Ny solid-state termisk diode udviklet med bedre ensretterydelse(a) og (b) repræsenterer for den skematiske geometri af den termiske diode bestående af Ni0.85Fe0.15S og Al2O3 for fremadgående og tilbagegående retning. (c) Termisk ensretningsfaktor (γ) som funktion -
 Komprimerende forskydning kan starte liv på andre planeterEn ny beregningsmodel af roterende diamantamboltcelleeksperimenter forudsiger, at kompressive forskydningskræfter udøvet af tidevandstrækket fra jovianske planeter på måner som Europa og Enceladus kan
Komprimerende forskydning kan starte liv på andre planeterEn ny beregningsmodel af roterende diamantamboltcelleeksperimenter forudsiger, at kompressive forskydningskræfter udøvet af tidevandstrækket fra jovianske planeter på måner som Europa og Enceladus kan -
 Forskere udfolder hemmelig stabilitet af bøjede sugerørUMass Amherst materialeforskere, med kolleger hos Virginia Tech, mener, at deres er den første undersøgelse, der undersøger, hvordan og hvorfor strukturer som bøjelige sugerør og sammenklappelige hund
Forskere udfolder hemmelig stabilitet af bøjede sugerørUMass Amherst materialeforskere, med kolleger hos Virginia Tech, mener, at deres er den første undersøgelse, der undersøger, hvordan og hvorfor strukturer som bøjelige sugerør og sammenklappelige hund -
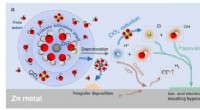 Hydrerede eutektiske elektrolytter hjælper med at forbedre ydeevnen af vandige zinkbatterierSkematiske diagrammer af Zn 2+ solvationsstruktur og grænsefladereaktioner i (a) traditionel vandig elektrolyt og (b) hydratiseret eutektisk elektrolyt. Kredit:Zhao Jingwen og Yang Wuhai Zink (Z
Hydrerede eutektiske elektrolytter hjælper med at forbedre ydeevnen af vandige zinkbatterierSkematiske diagrammer af Zn 2+ solvationsstruktur og grænsefladereaktioner i (a) traditionel vandig elektrolyt og (b) hydratiseret eutektisk elektrolyt. Kredit:Zhao Jingwen og Yang Wuhai Zink (Z
- Hvad er koncentrationen af hydroxidion i betragtning af det hydronium 1,5x10-5M?
- Er et kloratom eller ion større?
- Hvad er månens vinkeldiameter lige over horisonten?
- Hvordan regnbuer virker
- Hvordan strømmer energi gennem et elektromagnetisk kredsløb?
- Taler du til mig? Forskere forsøger at opklare mysteriet om 'dyresamtaler'


