Hvilket ville sænke frysepunktet mere 100 mol sukker eller NaCl?
Forståelse af kolligative egenskaber
Frysepunktdepression er en colligativ egenskab, hvilket betyder, at det afhænger af antallet af opløste partikler i en opløsning, ikke deres specifikke identitet.
* dissociation: NaCl (natriumchlorid) er en ionisk forbindelse, der adskiller sig i to ioner (Na+ og Cl-), når det opløses i vand.
* ikke-dissociation: Sukker (saccharose) er en kovalent forbindelse og adskiller sig ikke i vand.
Virkningen af dissociation
Da NaCl dissocierer i to ioner, vil en 100-mol opløsning af NaCl have 200 mol partikler I opløsning. En 100-mol opløsning af sukker har kun 100 mol partikler .
Konklusion
100-mol-opløsningen af NaCI vil sænke frysepunktet mere end 100-mol opløsning af sukker, fordi den producerer dobbelt så mange partikler i opløsning.
 Varme artikler
Varme artikler
-
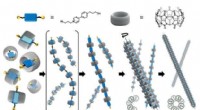 Selvsamlet kunstig mikrotubuli som LEGO byggeklodserHierarkisk selvsamling af polypseudorotaxaner til kunstige mikrotubuli. Kredit:Kimoon Kim (POSTECH) Simple LEGO klodser kan samles til mere komplicerede strukturer, som yderligere kan associeres t
Selvsamlet kunstig mikrotubuli som LEGO byggeklodserHierarkisk selvsamling af polypseudorotaxaner til kunstige mikrotubuli. Kredit:Kimoon Kim (POSTECH) Simple LEGO klodser kan samles til mere komplicerede strukturer, som yderligere kan associeres t -
 Sunde organeller, sunde cellerNøglecellulære processer finder sted i dråber dannet af RNA-molekyler og fluorescensmærket protein. Kredit:Maria Hondele/ETH Zürich. Det er for nylig blevet klart, hvor vigtige membranløse organel
Sunde organeller, sunde cellerNøglecellulære processer finder sted i dråber dannet af RNA-molekyler og fluorescensmærket protein. Kredit:Maria Hondele/ETH Zürich. Det er for nylig blevet klart, hvor vigtige membranløse organel -
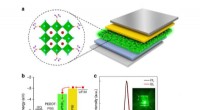 Ny tilgang til forbedring af perovskitfilmers stabilitet og optiske egenskabera) Enhedsstruktur og et tilsvarende tværsnits-TEM-billede af flerlags PeLEDerne; b) Skematisk fladbånds energidiagram over PeLED; c) Normaliseret fotoluminescensspektrum af CsPbBr3 -filmen, og elektro
Ny tilgang til forbedring af perovskitfilmers stabilitet og optiske egenskabera) Enhedsstruktur og et tilsvarende tværsnits-TEM-billede af flerlags PeLEDerne; b) Skematisk fladbånds energidiagram over PeLED; c) Normaliseret fotoluminescensspektrum af CsPbBr3 -filmen, og elektro -
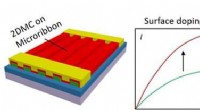 2-D molekylære krystaller, der modulerer elektroniske egenskaber af organiske halvledereSkema af den nederste port, topkontakt OFETer baseret på 1D/2D sammensatte enkeltkrystaller og skematisk diagram af I-V kurver før og efter doping. Kredit:Science China Press Organiske felteffektt
2-D molekylære krystaller, der modulerer elektroniske egenskaber af organiske halvledereSkema af den nederste port, topkontakt OFETer baseret på 1D/2D sammensatte enkeltkrystaller og skematisk diagram af I-V kurver før og efter doping. Kredit:Science China Press Organiske felteffektt
- Hvordan adskiller sig Veiws of Science and Church?
- Landformen, der bedst beskriver koldt klima?
- Bruger en glødepære og en let pind den samme form for energi til at skabe lys?
- Hvorfor kontrolleres nogle af flere alleler eller gener?
- Hvad er et arrangement af mineraler i flade eller bølgede parallelle bånd?
- Klimaændringer kan ændre den måde, havbølger påvirker 50 % af verdens kyster


