Hvilken er mere polære H2S eller H2O?
polaritet bestemmes af forskellen i elektronegativitet mellem atomerne i et molekyle. Elektronegativitet er et atoms evne til at tiltrække elektroner mod sig selv i en kemisk binding.
* ilt (O) er mere elektronegativ end svovl (r) .
* I H₂O tiltrækker iltatomet de delte elektroner stærkere end hydrogenatomerne, hvilket skaber en delvis negativ ladning på iltatomet og delvis positive ladninger på brintatomerne. Dette skaber et dipolmoment , hvilket gør vand til et polært molekyle.
* I H₂S er svovlatomet mindre elektronegativ end ilt, hvilket resulterer i en mindre forskel i elektronegativitet. Dette skaber et mindre dipolmoment, hvilket gør hydrogensulfid A mindre polært molekyle .
Derfor er H₂O mere polær end H₂s.
 Varme artikler
Varme artikler
-
 Et skridt nærmere biotekniske erstatninger for skibe og kanalerKredit:CC0 Public Domain Et team af forskere fra Brigham og Womens Hospital har udviklet en måde at bioprinte rørformede strukturer på, der bedre efterligner oprindelige kar og kanaler i kroppen.
Et skridt nærmere biotekniske erstatninger for skibe og kanalerKredit:CC0 Public Domain Et team af forskere fra Brigham og Womens Hospital har udviklet en måde at bioprinte rørformede strukturer på, der bedre efterligner oprindelige kar og kanaler i kroppen. -
 Registrering af forurening med en kompakt laserkildeKredit:Ecole Polytechnique Federale de Lausanne (EPFL) Forskere ved EPFL er kommet med en ny mellem infrarød lyskilde, der kan registrere drivhusgasser og andre gasser, samt molekyler i en persons
Registrering af forurening med en kompakt laserkildeKredit:Ecole Polytechnique Federale de Lausanne (EPFL) Forskere ved EPFL er kommet med en ny mellem infrarød lyskilde, der kan registrere drivhusgasser og andre gasser, samt molekyler i en persons -
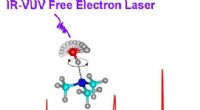 Forskere afslører dynamisk kobling af stærk hydrogenbindingAbstrakt https://doi.org/10.1021/acs.jpclett.1c00168 Hydrogenbindinger (HBer), de vigtigste intermolekylære interaktioner, er iboende svingende i naturen. At belyse de dynamiske koblinger af hydr
Forskere afslører dynamisk kobling af stærk hydrogenbindingAbstrakt https://doi.org/10.1021/acs.jpclett.1c00168 Hydrogenbindinger (HBer), de vigtigste intermolekylære interaktioner, er iboende svingende i naturen. At belyse de dynamiske koblinger af hydr -
 Hvor ren er din patchouli?Kredit:CC0 Public Domain Indonesisk patchouliolie repræsenterer en betydelig andel af verdensmarkedet, leverer omkring 90 procent til parfumeindustrien som et almindeligt fiksativmiddel til dufte.
Hvor ren er din patchouli?Kredit:CC0 Public Domain Indonesisk patchouliolie repræsenterer en betydelig andel af verdensmarkedet, leverer omkring 90 procent til parfumeindustrien som et almindeligt fiksativmiddel til dufte.
- Hvorfor er det vigtigt at spare atomenergi?
- Dristige undervandsmission afslører, hvor dybe havbundstrømme der kan rejse tusinder af kilometer
- Sporing af vandforurenende stoffer tilbage til kilden
- Hvad resulterede af at fodre søkøer med 100 tons salat? Embedsmænd overvejer lektier
- Teknologi, der detekterer RNase-aktivitet
- Hvordan blev Mælkevejen Galaxy dannet?


