Hvorfor smelter is, når salt tilsættes?
1. Depressionen for frysepunkt:
* Pure vand fryser ved 0 ° C (32 ° F). Dette skyldes, at vandmolekylerne arrangerer sig i en krystallinsk struktur.
* salt (NaCl) opløses i vand og nedbrydes i natrium (Na+) og chlorid (Cl-) ioner. Disse ioner forstyrrer det ordnede arrangement af vandmolekyler, hvilket gør det sværere for dem at fryse.
* Denne forstyrrelse sænker vandets frysepunkt. Jo mere salt du tilføjer, jo lavere bliver frysepunktet.
2. Hvordan salt smelter is:
* Når salt tilsættes til is, begynder det at opløses i det tynde vandlag, der altid findes på isens overflade.
* Denne opløsningsproces absorberer varme fra omgivelserne, inklusive selve isen. Denne absorption af varme hæver isens temperatur og smelter den.
* Salt opløses derefter i det smeltede vand, hvilket yderligere sænker frysepunktet. Dette betyder, at den omgivende is skal være endnu koldere for at fryse igen.
3. Hvorfor det fungerer bedre på is:
* salt fungerer bedst på is, fordi isen allerede har en lille mængde vand til stede. Dette gør det muligt for saltet at opløses let.
* salt smelter faktisk ikke is af sig selv. Det sænker simpelthen frysepunktet, så isen kan smelte ved en lavere temperatur, end den normalt ville.
Vigtig note: Mens salt er effektivt til at smelte is, kan det også være skadeligt for miljøet. Overdreven brug kan skade veje, vandveje og vegetation.
Sidste artikelHvad er H2O2 lavet af?
Næste artikelHvad er 3 elementer, der komponerer et atom?
 Varme artikler
Varme artikler
-
 Produktionsteknologi for nye flystrukturer har øget deres styrke3D-printede kompositdele. Kredit:Sergey Gnuskov/NUST MISIS Forskere fra NUST MISIS har udviklet en metode til fremstilling af kompositdele til luftfartsindustrien, som har øget styrken af færdige
Produktionsteknologi for nye flystrukturer har øget deres styrke3D-printede kompositdele. Kredit:Sergey Gnuskov/NUST MISIS Forskere fra NUST MISIS har udviklet en metode til fremstilling af kompositdele til luftfartsindustrien, som har øget styrken af færdige -
 Forskere opdager tilgang til at aktivere inerte gasserKredit:CC0 Public Domain Inerte gasser som argon danner typisk ikke kemiske bindinger undtagen under ekstreme forhold, såsom isens kolde kulde i det ydre rum. Som delt i Proceedings of the Nationa
Forskere opdager tilgang til at aktivere inerte gasserKredit:CC0 Public Domain Inerte gasser som argon danner typisk ikke kemiske bindinger undtagen under ekstreme forhold, såsom isens kolde kulde i det ydre rum. Som delt i Proceedings of the Nationa -
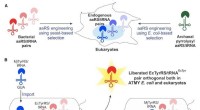 Konstrueret genetisk maskineri afledt af E. coli leverer nye aminosyrer til proteinerBoston College kemikere har udviklet en ny, bakterie-afledt teknologi til at inkorporere ikke-kanoniske aminosyrer i proteiner fra en bred klasse af organismer, inklusive mennesker. Kredit:Cell Chemic
Konstrueret genetisk maskineri afledt af E. coli leverer nye aminosyrer til proteinerBoston College kemikere har udviklet en ny, bakterie-afledt teknologi til at inkorporere ikke-kanoniske aminosyrer i proteiner fra en bred klasse af organismer, inklusive mennesker. Kredit:Cell Chemic -
 En ny sensor til lys, varme og berøringSensoren, der kan måle ændringer i kropstemperatur, og reagerer på både sollys og varm berøring. Kredit:Thor Balkhed Inspireret af opførsel af naturlig hud, forskere ved Laboratory of Organic Elec
En ny sensor til lys, varme og berøringSensoren, der kan måle ændringer i kropstemperatur, og reagerer på både sollys og varm berøring. Kredit:Thor Balkhed Inspireret af opførsel af naturlig hud, forskere ved Laboratory of Organic Elec


