Hvad sker der, når vandig brom tilsættes til natriumchlorid?
* Brom er mindre reaktiv end klor: Chlor er et stærkere oxidationsmiddel end brom. Dette betyder, at klor har en større tendens til at få elektroner og reduceres.
* Halogenerne følger tendensen med faldende reaktivitet ned i gruppen: Fluor er den mest reaktive, efterfulgt af klor, brom og jod.
* Ingen forskydningsreaktion: For at en reaktion kan forekomme, er brom nødt til at fortrænge klor fra NaCl. Brom er imidlertid mindre reaktiv og kan ikke fortrænge klor.
Derfor forbliver blandingen som separate vandige opløsninger af brom og natriumchlorid.
Mulig observation: Løsningen vil sandsynligvis have en gulbrun farve på grund af tilstedeværelsen af brom.
Bemærk: Selvom der ikke opstår nogen signifikant reaktion, hvis du skulle udsætte opløsningen for sollys eller UV -lys, kunne der produceres en lille mængde klorgas. Dette skyldes, at sollys kan give nok energi til at overvinde energibarrieren til, at en reaktion kan forekomme. Imidlertid er denne reaktion meget langsom og usandsynligt at være mærkbar under normale forhold.
Sidste artikelHvad er formlen for tetranitrogendifluorid?
Næste artikelHvilke mineraler har kun en retning af spaltning?
 Varme artikler
Varme artikler
-
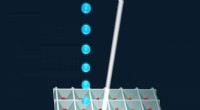 Happy hour for tidsopløst krystallografiLiquid Application Method for time-resolved Analyses (LAMA) åbner døren for alle diffusionsvenlige proteinkrystalsystemer. Kredit:Joerg M. Harms, MPSD Forskere fra Department of Atomically Resolve
Happy hour for tidsopløst krystallografiLiquid Application Method for time-resolved Analyses (LAMA) åbner døren for alle diffusionsvenlige proteinkrystalsystemer. Kredit:Joerg M. Harms, MPSD Forskere fra Department of Atomically Resolve -
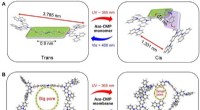 Mikroporøse polymermembraner til let-gatet iontransportSkematisk repræsentation af bottom-up designstrategien for konstruktion af kunstig lys-gatet ionkanalmembran. (A) Trans-cis-trans reversibel isomerisering af den syntetiserede azo-CMP-monomer og (B) d
Mikroporøse polymermembraner til let-gatet iontransportSkematisk repræsentation af bottom-up designstrategien for konstruktion af kunstig lys-gatet ionkanalmembran. (A) Trans-cis-trans reversibel isomerisering af den syntetiserede azo-CMP-monomer og (B) d -
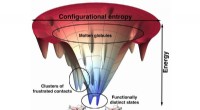 Atomopløsningsproteinmodeller afslører nye detaljer om proteinbindingAtomskalamodeller af Rice University-forskere baseret på dem, der bruges til at forudsige, hvordan proteiner folder, viser en stærk sammenhæng mellem minimalt frustrerede bindingssteder og lægemiddels
Atomopløsningsproteinmodeller afslører nye detaljer om proteinbindingAtomskalamodeller af Rice University-forskere baseret på dem, der bruges til at forudsige, hvordan proteiner folder, viser en stærk sammenhæng mellem minimalt frustrerede bindingssteder og lægemiddels -
 Forskere ser kemisk rækkevidde i mellem-entropi-legeringKredit:CC0 Public Domain Kinesiske forskere har foretaget direkte observationer af ansigtscentrerede kubiske VCoNi (medium) -entropylegeringer (MEA) og for første gang foreslået en overbevisende i
Forskere ser kemisk rækkevidde i mellem-entropi-legeringKredit:CC0 Public Domain Kinesiske forskere har foretaget direkte observationer af ansigtscentrerede kubiske VCoNi (medium) -entropylegeringer (MEA) og for første gang foreslået en overbevisende i


