Krystaller af den ioniske forbindelse Calciumfluor har en anden struktur end det chlorid?
* ionisk radius: Fluorioner (F⁻) er meget mindre end chloridioner (CL⁻). Denne forskel i ionisk radius påvirker signifikant pakningsarrangementet af ionerne i krystalgitteret.
* Koordinationsnummer: Den mindre størrelse af fluorioner gør det muligt for calcium at koordinere med et højere antal fluorioner. Dette resulterer i en anden krystalstruktur.
* struktur:
* calciumfluorid (CAF₂): Har en fluoritstruktur , hvor hver calciumion er omgivet af 8 fluorioner, og hver fluorionion er omgivet af 4 calciumioner.
* calciumchlorid (cacl₂): Har en rutil struktur , hvor hver calciumion er omgivet af 6 chloridioner, og hver chloridion er omgivet af 3 calciumioner.
Kortfattet: Forskellen i ioniske radier mellem fluorid og chloridioner fører til forskellige koordinationsnumre og i sidste ende forskellige krystalstrukturer til calciumfluorid og calciumchlorid.
 Varme artikler
Varme artikler
-
 Brug af lasere til at visualisere molekylære mysterier i vores atmosfæreMolekylær vekselvirkning mellem gasser og væsker understøtter meget af vores liv, men vanskeligheder med at måle gas-væske kollisioner har indtil videre forhindret den grundlæggende udforskning af dis
Brug af lasere til at visualisere molekylære mysterier i vores atmosfæreMolekylær vekselvirkning mellem gasser og væsker understøtter meget af vores liv, men vanskeligheder med at måle gas-væske kollisioner har indtil videre forhindret den grundlæggende udforskning af dis -
 Side-by-side afsætning af atomisk flade halvlederplader forbedrer solcellekonverteringseffektivitet…Solenergikonvertering ved hjælp af en lateral WSe2-MoS2 heterojunction. Kredit:© 2017 WILEY VCH Supertynde fotovoltaiske enheder understøtter solteknologien, og der søges derfor meget efter gevins
Side-by-side afsætning af atomisk flade halvlederplader forbedrer solcellekonverteringseffektivitet…Solenergikonvertering ved hjælp af en lateral WSe2-MoS2 heterojunction. Kredit:© 2017 WILEY VCH Supertynde fotovoltaiske enheder understøtter solteknologien, og der søges derfor meget efter gevins -
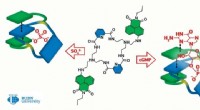 Kemikere skaber et molekyle, der kan hjælpe med at behandle hjertesygdomme og opdage viraKredit:RUDN Universitet RUDN University kemikere sammen med kolleger fra Chemnitz University of Technology (Tyskland) har syntetiseret den første kemiske receptor, der effektivt kan binde til cykl
Kemikere skaber et molekyle, der kan hjælpe med at behandle hjertesygdomme og opdage viraKredit:RUDN Universitet RUDN University kemikere sammen med kolleger fra Chemnitz University of Technology (Tyskland) har syntetiseret den første kemiske receptor, der effektivt kan binde til cykl -
 Stigning af mandlige individer i stingless bier kolonier fører til dronninger dødUndersøgelse tyder på fremkomsten af hanbier med både faderligt og moderligt genetisk materiale ubalancer arbejdsstyrke i kolonier af Scaptotrigona depilis (fysogastrisk dronning inspicerer yngelc
Stigning af mandlige individer i stingless bier kolonier fører til dronninger dødUndersøgelse tyder på fremkomsten af hanbier med både faderligt og moderligt genetisk materiale ubalancer arbejdsstyrke i kolonier af Scaptotrigona depilis (fysogastrisk dronning inspicerer yngelc
- Fælles edderkopper i Sydafrika
- Økologisk artsdannelse ved seksuel selektion på gode gener:Er adaptiv?
- Forskere opdager, hvorfor sten flyder langsomt i jordens midterkappe
- Kontrastmiddel til tumordiagnostik:Fosforescerende metal-organiske koordinationspolymerer til optisk…
- Hvilke ioner dannes, når ammoniak opløses i vand?
- Hvad er den videnskab, der registrerer fakta om jordoverfladen?


