Vand opløses mange ioniske og molekylære forbindelser på grund af dets hvad?
Her er hvorfor:
* vand er et polært molekyle: Oxygenatomet i vand er mere elektronegativ end hydrogenatomerne, hvilket betyder, at det tiltrækker elektroner stærkere. Dette skaber en delvis negativ ladning på ilt og delvis positive ladninger på hydrogenerne, hvilket gør molekylet polært.
* ioniske forbindelser holdes sammen af elektrostatiske kræfter: Disse kræfter er stærke, men de kan forstyrres af polære molekyler som vand. Det delvist negative ilt i vand tiltrækker de positive ioner i den ioniske forbindelse, og de delvist positive hydrogener tiltrækker de negative ioner. Denne attraktion svækker de elektrostatiske kræfter, der holder den ioniske forbindelse sammen, hvilket får den til at opløses.
* polære molekyler opløses i polære opløsningsmidler: Vand er et polært opløsningsmiddel, og det kan opløse andre polære molekyler som sukker og alkoholer. De delvise ladninger på vandmolekylet interagerer med de delvise ladninger på de polære molekyler, hvilket får dem til at opløses.
Kortfattet: Vands polaritet giver det mulighed for at interagere med både ioniske og polære molekyler, forstyrre deres bindinger og opløse dem.
Sidste artikelHvorfor er natriumcitrat i rengøringsprodukter?
Næste artikelHvad er isomeren af eddikesyre?
 Varme artikler
Varme artikler
-
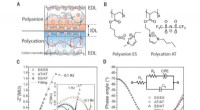 Ionotronisk teknologi, der ikke kræver flydende elektrolytterDannelse af en IDL ved grænsefladen mellem to modsat ladede ionoelastomerer. (A) Skematisk illustration af en polyanion/polykation-forbindelse. Kulstof-nanorørelektroder med stort overfladeareal er in
Ionotronisk teknologi, der ikke kræver flydende elektrolytterDannelse af en IDL ved grænsefladen mellem to modsat ladede ionoelastomerer. (A) Skematisk illustration af en polyanion/polykation-forbindelse. Kulstof-nanorørelektroder med stort overfladeareal er in -
 Hvordan en vietnamesisk rå svinekødssnack kunne hjælpe os med at holde maden frisk, naturligtVietnamesisk fermenteret svinekødssnack, Nem Chua. Kredit:RMIT University En traditionel vietnamesisk kødsnack kunne indeholde nøglen til at udvikle et sikkert og naturligt fødevarekonserveringsmi
Hvordan en vietnamesisk rå svinekødssnack kunne hjælpe os med at holde maden frisk, naturligtVietnamesisk fermenteret svinekødssnack, Nem Chua. Kredit:RMIT University En traditionel vietnamesisk kødsnack kunne indeholde nøglen til at udvikle et sikkert og naturligt fødevarekonserveringsmi -
 Ny teknik kan hjælpe med at konstruere forurenet vandfilter, menneskeligt vævBlomstformede biomaterialer ved hjælp af konstruerede proteinbyggesten. Kredit:Nancy Hernandez, William Hansen og Slava Manichev Forskere kan forvandle proteiner til uendelige mønstre, der ligner
Ny teknik kan hjælpe med at konstruere forurenet vandfilter, menneskeligt vævBlomstformede biomaterialer ved hjælp af konstruerede proteinbyggesten. Kredit:Nancy Hernandez, William Hansen og Slava Manichev Forskere kan forvandle proteiner til uendelige mønstre, der ligner -
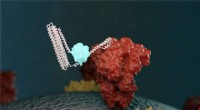 Nye biosensorer opdager hurtigt coronavirus -proteiner og antistofferEn illustration af en ny biosensor, der binder sig til et målrettet molekyle og udsender lys. Oprettelsen af biosensoren blev ledet af UW Medicine Institute for Protein Design. Kredit:Ian Haydon/UW
Nye biosensorer opdager hurtigt coronavirus -proteiner og antistofferEn illustration af en ny biosensor, der binder sig til et målrettet molekyle og udsender lys. Oprettelsen af biosensoren blev ledet af UW Medicine Institute for Protein Design. Kredit:Ian Haydon/UW
- Hvorfor himmel vises blå midt på dagen?
- Den type jord, der findes på Deccan Plateau?
- Hvorfor lugter saltsyre natriumsulfid som æg?
- Supercomputere kan få øje på cybertrusler
- Hvilken idé foreslog Max Planck at hjælpe med at forklare, hvorfor en sortkrops radiator ikke afga…
- Hvorfor at studere kunst som skuespil eller dans bedre kan ruste handelsstuderende til post-COVID-ve…


