Hvad er den molekylære og nettoioniske ligning af bariumhydroxid -hydrocyansyre?
1. Molekylær ligning
* reaktanter: Bariumhydroxid (BA (OH) ₂) og hydrocyansyre (HCN)
* Produkter: Bariumcyanid (BA (CN) ₂) og vand (H₂O)
molekylær ligning:
BA (OH) ₂ (aq) + 2HCN (aq) → Ba (CN) ₂ (aq) + 2H₂O (l)
2. Nettoionisk ligning
* Identificer de stærke elektrolytter: Bariumhydroxid, hydrocyansyre og bariumcyanid er stærke elektrolytter.
* Skriv den komplette ioniske ligning: Opdel de stærke elektrolytter i deres ioner.
* Annuller tilskuerionerne: Tilskuerioner vises på begge sider af ligningen og deltager ikke i reaktionen.
Komplet ionisk ligning:
Ba²⁺ (aq) + 2OH⁻ (aq) + 2H⁺ (aq) + 2cn⁻ (aq) → ba²⁺ (aq) + 2cn⁻ (aq) + 2h₂o (l)
nettoionisk ligning:
2OH⁻ (aq) + 2H⁺ (aq) → 2H₂O (l)
forenklet netto ionisk ligning:
OH⁻ (aq) + H⁺ (aq) → H₂O (L)
Vigtig note: Hydrocyansyre (HCN) er en svag syre, men den behandles som en stærk elektrolyt i dette tilfælde, fordi reaktionen er drevet af dannelsen af vand.
Sidste artikelHvad er størrelsen på et svovlatom?
Næste artikelEt atom af silicium kan kombineres korrekt i en forbindelse med?
 Varme artikler
Varme artikler
-
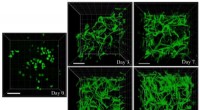 Biopolymerer til sårbehandling leverer stamceller for at forbedre helingenFigur viser det celleledende miljø af gellangummi-kollagen IPN-hydrogeler. De indkapslede fedtafledte mesenkymale stamceller (ADSCer) udviser gradvis tilbagevenden af morfologi til deres sædvanlige
Biopolymerer til sårbehandling leverer stamceller for at forbedre helingenFigur viser det celleledende miljø af gellangummi-kollagen IPN-hydrogeler. De indkapslede fedtafledte mesenkymale stamceller (ADSCer) udviser gradvis tilbagevenden af morfologi til deres sædvanlige -
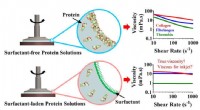 Fundning af fibrøst protein kan føre til forbedret bioprintning, vævsteknikKollagen og fibrinogen i vandige opløsninger danner et fast lag på overfladen af vand, ødelægger målinger af flowadfærd med rotationsreometere. Tilsætning af et ikke-ionisk overfladeaktivt stof i sm
Fundning af fibrøst protein kan føre til forbedret bioprintning, vævsteknikKollagen og fibrinogen i vandige opløsninger danner et fast lag på overfladen af vand, ødelægger målinger af flowadfærd med rotationsreometere. Tilsætning af et ikke-ionisk overfladeaktivt stof i sm -
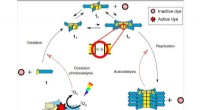 Livsemulerende molekyler viser grundlæggende stofskifteArbejdet fra Otto-lab har resulteret i et kemisk system, der viser forskellige egenskaber ved livet. Gennem oxidation, grundlæggende byggeklodser samles for at danne ringe i forskellige størrelser (ve
Livsemulerende molekyler viser grundlæggende stofskifteArbejdet fra Otto-lab har resulteret i et kemisk system, der viser forskellige egenskaber ved livet. Gennem oxidation, grundlæggende byggeklodser samles for at danne ringe i forskellige størrelser (ve -
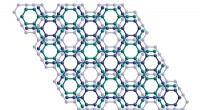 Langhypoteseret næste generations vidundermateriale skabt for første gangKrystalstrukturen af et lag af grafyn. Kredit:Yiming Hu I over et årti har forskere forsøgt at syntetisere en ny form for kulstof kaldet grafyn med begrænset succes. Den bestræbelse er dog nu ved
Langhypoteseret næste generations vidundermateriale skabt for første gangKrystalstrukturen af et lag af grafyn. Kredit:Yiming Hu I over et årti har forskere forsøgt at syntetisere en ny form for kulstof kaldet grafyn med begrænset succes. Den bestræbelse er dog nu ved
- Ville en dyb jordvandscyklus ændre vores forståelse af planetarisk evolution?
- Hvad er sammensætningen af Mesosphere mantle?
- Raket til at se solen med røntgensyn
- Payne-Gaposchkin,
- Kunne det samme materiale bruges både en leder og en isolator?
- Forskning i biovåben er forbudt i henhold til en international traktat, men ingen tjekker for overt…


