Ved dannelse af en kemisk forbindelse får et atom af elementforstærkning eller mister elektroner?
* ioniske forbindelser: I disse forbindelser mister et atom Elektroner (bliver en positivt ladet kation) og det andet atom gains Elektroner (bliver en negativt ladet anion). Denne overførsel af elektroner skaber en elektrostatisk attraktion, der holder ionerne sammen.
* Eksempel:Natrium (NA) mister et elektron for at blive Na⁺, mens klor (CL) får et elektron for at blive Cl⁻. De danner den ioniske forbindelse natriumchlorid (NaCl).
* kovalente forbindelser: I disse forbindelser deler atomer Elektroner snarere end at overføre dem fuldstændigt. De delte elektroner tiltrækkes af kernerne i begge atomer og holder atomerne sammen.
* Eksempel:I metan (CH₄) deler kulstof sine fire valenselektroner med fire hydrogenatomer, hvilket skaber fire kovalente bindinger.
Kortfattet:
* ioniske forbindelser: Gevinst og tab af elektroner.
* kovalente forbindelser: Deling af elektroner.
Det er vigtigt at huske, at nogle elementer kan deltage i både ionisk og kovalent binding afhængigt af de andre elementer, de binder til.
 Varme artikler
Varme artikler
-
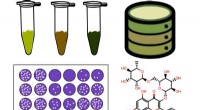 Et stof, der findes i brunkul, kan hjælpe med at bekæmpe viraAntiviral aktivitet af ti humusstofprøver (HS) blev vurderet mod flåtbåren encephalitisvirus reproduktion. For at afsløre mulige aktive komponenter i HS -prøver blev der søgt efter FTICR MS -data i Ch
Et stof, der findes i brunkul, kan hjælpe med at bekæmpe viraAntiviral aktivitet af ti humusstofprøver (HS) blev vurderet mod flåtbåren encephalitisvirus reproduktion. For at afsløre mulige aktive komponenter i HS -prøver blev der søgt efter FTICR MS -data i Ch -
 Ny type plast fremstillet af genvundet affaldSammensat og granuleret polyhydroxybutyrat (PHB). Kredit:Fraunhofer-Gesellschaft En ny type plast fremstillet af genvundet affald nedbrydes let på mindre end et år. Det stof, der snart vil tjene t
Ny type plast fremstillet af genvundet affaldSammensat og granuleret polyhydroxybutyrat (PHB). Kredit:Fraunhofer-Gesellschaft En ny type plast fremstillet af genvundet affald nedbrydes let på mindre end et år. Det stof, der snart vil tjene t -
 Ny strategi forbedrer aromatiske selektivitet i metankonverteringMeget forbedret aromatisk selektivitet ved kobling af chlormethan og carbonmonoxid over H-ZSM-5. Kredit:Fang Xudong Metan, hovedbestanddelen i skifergas og brændbar is, forventes at erstatte petrol
Ny strategi forbedrer aromatiske selektivitet i metankonverteringMeget forbedret aromatisk selektivitet ved kobling af chlormethan og carbonmonoxid over H-ZSM-5. Kredit:Fang Xudong Metan, hovedbestanddelen i skifergas og brændbar is, forventes at erstatte petrol -
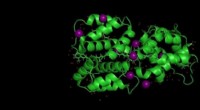 Vores første kig på et nyt lysabsorberende protein i cyanobakterierKredit:Michigan State University Cyanobakterier er små, hårdføre organismer. Hver celle er 25 gange mindre end et menneskehår, men lad ikke størrelsen narre dig. Deres kollektive evne til at udvid
Vores første kig på et nyt lysabsorberende protein i cyanobakterierKredit:Michigan State University Cyanobakterier er små, hårdføre organismer. Hver celle er 25 gange mindre end et menneskehår, men lad ikke størrelsen narre dig. Deres kollektive evne til at udvid


