Kan eller skal natriumhydroxid anvendes til at neutralisere hydrofluorinsyre?
Årsag:
* HF er en svag syre, men den er meget ætsende og reagerer voldsomt med NaOH. Reaktionen genererer en betydelig mængde varme, som kan føre til en løbsk reaktion og eksplosion.
* HF kan trænge ind i huden og reagere med calcium i knoglerne, hvilket forårsager alvorlige forbrændinger og potentielle knogleskader. NaOH kan også forårsage alvorlige hudforbrændinger.
* Reaktionen mellem HF og NaOH producerer natriumfluorid (NAF), som også er giftig.
Sikker neutraliseringsmetoder til HF:
* calciumhydroxid (CA (OH) 2): Calciumhydroxid reagerer med HF for at danne calciumfluorid (CAF2), som er mindre opløselig og mindre giftig end NAF.
* magnesiumoxid (MGO): Magnesiumoxid reagerer med HF for at danne magnesiumfluorid (MGF2), som også er mindre opløselig og mindre giftig end NAF.
* natriumbicarbonat (NAHCO3): Natriumbicarbonat kan bruges i små mængder til at neutralisere små spild af HF, men det er mindre effektivt end Ca (OH) 2 eller MGO.
Vigtige overvejelser:
* Brug altid passende personligt beskyttelsesudstyr (PPE), inklusive handsker, beskyttelsesbriller og en åndedrætsværn.
* neutraliser HF-spild i et godt ventileret område.
* Forsøg aldrig at neutralisere HF uden ordentlig træning og sikkerhedsforholdsregler.
* Hvis HF kommer i kontakt med hud, skal du straks skylle området med rigelige mængder vand i mindst 15 minutter.
Konklusion:
På grund af de betydelige farer, der er forbundet med at bruge NaOH til at neutralisere HF, er det stærkt modløs. Alternative neutraliseringsmetoder, såsom calciumhydroxid eller magnesiumoxid, er sikrere og mere effektive. Prioriter altid sikkerhed og følg ordentlige procedurer, når du håndterer HF.
Sidste artikelHvad er den kemiske formel for kobber II bromid?
Næste artikelAngiv antallet af valenselektroner i et atomkalcium?
 Varme artikler
Varme artikler
-
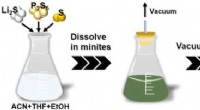 Udvikling af en ny storstilet fremstillingsteknologi til faste sulfidelektrolytterSkema af den nye løsningsbehandlingsteknologi for sulfid SEer. Kredit:Toyohashi University of Technology En forskergruppe i ph.d.-programmet ved Toyohashi University of Technologys afdeling for ele
Udvikling af en ny storstilet fremstillingsteknologi til faste sulfidelektrolytterSkema af den nye løsningsbehandlingsteknologi for sulfid SEer. Kredit:Toyohashi University of Technology En forskergruppe i ph.d.-programmet ved Toyohashi University of Technologys afdeling for ele -
 Ny hybrid 3D-printteknik vil tilføje en fjerde dimension til additiv fremstillingGrafisk abstrakt. Kredit:DOI:10.1016/j.addma.2021.102337 En ny kemisk proces til additiv fremstilling antyder spændende muligheder for 4D-printede komponenter – såsom egenskaber, der ændrer sig ov
Ny hybrid 3D-printteknik vil tilføje en fjerde dimension til additiv fremstillingGrafisk abstrakt. Kredit:DOI:10.1016/j.addma.2021.102337 En ny kemisk proces til additiv fremstilling antyder spændende muligheder for 4D-printede komponenter – såsom egenskaber, der ændrer sig ov -
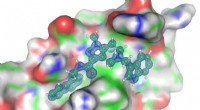 Ny terapeutisk strategi mod sovesygeStruktur af grænsefladen mellem PEX14 og PEX5 (bagpå) inklusive strukturen af inhibitoren (foran). Kredit:Dr. Grzegorz Popowicz, Helmholtz Zentrum München Et nyudviklet lille molekyle dræber sel
Ny terapeutisk strategi mod sovesygeStruktur af grænsefladen mellem PEX14 og PEX5 (bagpå) inklusive strukturen af inhibitoren (foran). Kredit:Dr. Grzegorz Popowicz, Helmholtz Zentrum München Et nyudviklet lille molekyle dræber sel -
 Et nyt potentielt alternativ til myggebekæmpelse opdagetKredit:CC0 Public Domain Naturlige æteriske olier udvundet af skallen af en citrusfrugt kunne være et effektivt nyt miljøvenligt alternativ i myggekontrolprogrammer, rapporterer en ny undersøgel
Et nyt potentielt alternativ til myggebekæmpelse opdagetKredit:CC0 Public Domain Naturlige æteriske olier udvundet af skallen af en citrusfrugt kunne være et effektivt nyt miljøvenligt alternativ i myggekontrolprogrammer, rapporterer en ny undersøgel
- Hvordan kan du teste et ukendt krystallinsk stof for at afgøre, om det er bordsalt?
- Undersøgelse tyder på, at træer er afgørende for vores byers fremtid
- Bioøkonomier sigter mod at blive et bankende hjerte i lokalsamfund, både landdistrikterne og byern…
- Er nord til syd for ækvatorlængdegrad?
- Et nyt spin på datalagring med lav effekt:Små ferromagneter med ultratynde isolerende lag
- I første, Scientific American-magasinet støtter Biden


