Hvorfor opløses natrium i vand, men kobber ikke?
natrium (NA):
* reaktivitet: Natrium er et meget reaktivt alkalimetal. Det mister let sit yderste elektron for at danne en positivt ladet ion (Na+).
* reaktion med vand: Når natrium kommer i kontakt med vand, forekommer en kraftig reaktion. Natriumatomet donerer sit elektron til et vandmolekyle og danner en natriumion (Na+) og en hydroxidion (OH-). Denne reaktion frigiver en betydelig mængde energi, hvilket ofte får natrium til at smelte og endda antænde.
* Dannelse af natriumhydroxid: Natriumionerne og hydroxidionerne reagerer yderligere på dannelse af natriumhydroxid (NaOH), som er opløselig i vand. Dette opløser natriumet fuldstændigt.
kobber (CU):
* lavere reaktivitet: Kobber er et overgangsmetal og er mindre reaktivt end natrium. Det holder fast på sine elektroner tættere.
* Ingen signifikant reaktion: Mens kobber kan reagere med visse syrer (som salpetersyre), reagerer det ikke let med vand. Reaktionen med vand er ikke energisk gunstig nok til at overvinde den stærke metalliske binding i kobber.
* Oxidation: Kobber oxideres (reagerer med ilt) i nærvær af luft og fugt og danner en grøn patina (kobberoxid). Denne patina fungerer som et beskyttende lag og forhindrer yderligere oxidation.
Kortfattet: Natrium opløses i vand på grund af dets høje reaktivitet og dens tendens til at danne ioner, der let opløses i vand. Kobber, der er mindre reaktiv, gennemgår ikke en betydelig reaktion med vand, og dens oxidation i luft danner et beskyttende lag, der forhindrer yderligere reaktion.
Sidste artikelHvad er tilstanden af svovl?
Næste artikelHvorfor bruges svovldioxid til vinfremstilling?
 Varme artikler
Varme artikler
-
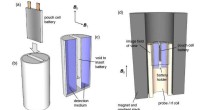 Kemikere udvikler MRI-lignende teknik til at opdage, hvad der fejler batterierEt team af kemikere har udviklet en MRI-baseret teknik, der hurtigt kan diagnosticere, hvad der fejler visse typer batterier - fra at bestemme, hvor meget ladning der er tilbage til at opdage interne
Kemikere udvikler MRI-lignende teknik til at opdage, hvad der fejler batterierEt team af kemikere har udviklet en MRI-baseret teknik, der hurtigt kan diagnosticere, hvad der fejler visse typer batterier - fra at bestemme, hvor meget ladning der er tilbage til at opdage interne -
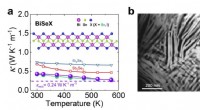 Ekstremt lav varmeledningsevne i 1-D blød kædestruktur(a) Den termiske ledningsevne som funktion af temperaturen. Insert er kædestrukturen af BiSeI. (b) Morfologien af trådformede kæder i 1D BiSeI. Kredit:©Science China Press Forskere har rapport
Ekstremt lav varmeledningsevne i 1-D blød kædestruktur(a) Den termiske ledningsevne som funktion af temperaturen. Insert er kædestrukturen af BiSeI. (b) Morfologien af trådformede kæder i 1D BiSeI. Kredit:©Science China Press Forskere har rapport -
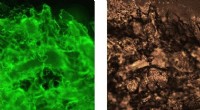 Forskere udvikler gel lavet af edderkoppesilkeproteiner til biomedicinske anvendelserHydrogelerne farves med et fluorescerende farvestof, der binder til amyloidstrukturer og det tilsvarende lysfeltbillede. Kredit:Tina Arndt Forskere ved KI og SLU har opdaget, at edderkoppesilkeprot
Forskere udvikler gel lavet af edderkoppesilkeproteiner til biomedicinske anvendelserHydrogelerne farves med et fluorescerende farvestof, der binder til amyloidstrukturer og det tilsvarende lysfeltbillede. Kredit:Tina Arndt Forskere ved KI og SLU har opdaget, at edderkoppesilkeprot -
 Halvlederchip, der detekterer udåndet gas med høj følsomhed ved stuetemperaturIoT kemisk sensor, der registrerer små mængder gasmolekyler, der er adsorberet på overfladen af det tynde nanosheet Kredit:Toyohashi University of Technology. Tredjeårs doktorand Toshiaki Takaha
Halvlederchip, der detekterer udåndet gas med høj følsomhed ved stuetemperaturIoT kemisk sensor, der registrerer små mængder gasmolekyler, der er adsorberet på overfladen af det tynde nanosheet Kredit:Toyohashi University of Technology. Tredjeårs doktorand Toshiaki Takaha
- Vind er et eksempel på hvilken energi?
- Hvem har skylden, når iCloud 'hackede' - dig eller Apple?
- Undersøgelse:Ældre bilister har brug for mere tid til at reagere på vejfarer
- Hvorfor afgiver solen en enorm mængde solenergi?
- Ny anisotropisk ledende film til monteringsapplikationer med ultrafin pitch
- Hvad er fysikbegrebet Ferris Wheel i fortryllet rige?


