Hvorfor opløses iod let i CCL4?
* jod: Jodmolekyler er ikke -polære og holdes sammen af London Dispersion Forces (svage midlertidige dipoler).
* carbon tetrachlorid: CCL₄ er også et ikke -polært molekyle, der primært holdes sammen af London Dispersion Forces .
Hvorfor dette betyder noget:
* som opløser som: Dette princip siger, at polære opløsningsmidler opløser polære opløste stoffer, og ikke -polære opløsningsmidler opløser ikke -polære opløste stoffer.
* Intermolekylær kraftkompatibilitet: Da både jod- og carbontetrachlorid er ikke -polære, er deres London -spredningskræfter kompatible. De kan interagere med hinanden, hvilket tillader, at jodmolekylerne kan sprede jævnt i hele CCL₄ -opløsningsmidlet.
I modsætning:
* Jod er uopløselig i vand (H₂O), et polært opløsningsmiddel. Dette skyldes, at den stærke hydrogenbinding i vand ikke effektivt kan interagere med de ikke -polære iodmolekyler.
Nøgle takeaways:
* Opløseligheden af et stof afhænger af styrken og typen af intermolekylære kræfter, der er til stede i både opløst og opløsningsmiddel.
* Ikke -polære opløsningsmidler, som carbontetrachlorid, er gode opløsningsmidler til ikke -polære opløste stoffer, som jod.
* Polære opløsningsmidler, som vand, er gode opløsningsmidler til polære opløste stoffer.
Sidste artikelHvorfor er jod mere opløselig i parafin end vand?
Næste artikelHvor mange atom i 1 g molybdæn?
 Varme artikler
Varme artikler
-
 Kuldioxidreaktor laver brændstof fra MarsUniversity of Cincinnati kemiingeniørstuderende Tianyu Zhang holder et hætteglas med grafen op, der bruges som katalysator til at omdanne kuldioxid til metan. Kredit:Andrew Higley/UC Creative Inge
Kuldioxidreaktor laver brændstof fra MarsUniversity of Cincinnati kemiingeniørstuderende Tianyu Zhang holder et hætteglas med grafen op, der bruges som katalysator til at omdanne kuldioxid til metan. Kredit:Andrew Higley/UC Creative Inge -
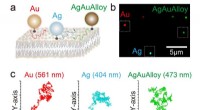 Hurtig og præcis flerfarvebilleddannelse af biomolekyler nu muligBrugen af guld, sølv og guld-sølv legering nanopartikler tillod højhastigheds/høj præcision flerfarve billeddannelse for første gang. Kredit:Ryota Iino, Institut for Molekylær Videnskab, National In
Hurtig og præcis flerfarvebilleddannelse af biomolekyler nu muligBrugen af guld, sølv og guld-sølv legering nanopartikler tillod højhastigheds/høj præcision flerfarve billeddannelse for første gang. Kredit:Ryota Iino, Institut for Molekylær Videnskab, National In -
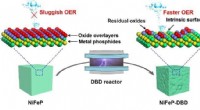 Ætseprocessen øger udvindingen af brint under vandelektrolyseSkematisk diagram over ætsningsprocessen, der anvendes på metalphosphidelektrokatalysatorer. Kredit:Forfatterne Udvinding af brint fra vand gennem elektrolyse er en lovende vej til at øge produkti
Ætseprocessen øger udvindingen af brint under vandelektrolyseSkematisk diagram over ætsningsprocessen, der anvendes på metalphosphidelektrokatalysatorer. Kredit:Forfatterne Udvinding af brint fra vand gennem elektrolyse er en lovende vej til at øge produkti -
 At skabe unikke konstruktioner fra metalmembranerCykelbanen Krylatskoye - sportsanlæg i Moskva, i Krylatskoye-distriktet. Kredit:Sergey Krivoshapko RUDN University Professor Sergey Krivoshapko har assimileret information om metalmembran-ophængte
At skabe unikke konstruktioner fra metalmembranerCykelbanen Krylatskoye - sportsanlæg i Moskva, i Krylatskoye-distriktet. Kredit:Sergey Krivoshapko RUDN University Professor Sergey Krivoshapko har assimileret information om metalmembran-ophængte
- Forvandling af bilplastik til skum med kokosolie
- Hvordan hemmelighederne bag tardigrad kunne forbedre livreddende lægemidler som insulin
- Hvad er den kemiske forbindelse SnH2?
- Hvorfor observatorier placeret højt oppe i bjergene?
- Forskning kvantificerer kløften i kulstoffjernelse for første gang - viser, at lande har brug for …
- Hvad asorberer energien, der udstråles fra overfladen?


