Hvorfor skal du bruge et frisklavet ironii -sulfat i vores laboratorieeksperiment?
* jern (II) -ioner (Fe²⁺) oxideres let til jern (III) ioner (Fe³⁺): I nærvær af ilt og vand reagerer sulfat let med ilt for at danne jern (III) sulfat (Fe₂ (SO₄) ₃) og andre jern (III) forbindelser. Denne oxidationsproces accelereres af faktorer som lys, varme og tilstedeværelsen af urenheder.
* jern (III) sulfat har forskellige kemiske egenskaber: Jern (III) sulfat opfører sig anderledes end jern (II) sulfat i kemiske reaktioner. Brug af en oxideret opløsning ville føre til unøjagtige resultater og potentielt forstyrre den ønskede reaktion.
Her er, hvordan frisk forberedelse hjælper:
* minimerer oxidation: Ved at forberede opløsningen umiddelbart før brug minimerer du tidsjern (II) -ioner udsættes for ilt og vand, hvilket reducerer chancen for oxidation.
* sikrer nøjagtig støkiometri: Frisk tilberedte opløsninger sikrer den nøjagtige koncentration af jern (II) -ioner er kendt, hvilket fører til mere nøjagtige og reproducerbare resultater i dit eksperiment.
Sammenfattende er det afgørende for at sikre, at opløsningen indeholder det ønskede jern (II) -ioner og for at undgå interferens fra oxidationsprodukter. ved at bruge et frisklavet jern (II) sulfatopløsning.
Sidste artikelHvad er ladningen på jernholdig ion i sulfat?
Næste artikelHvorfor kan svovl ikke bruges til at fremstille ledninger?
 Varme artikler
Varme artikler
-
 Fotokrome vismutkomplekser viser et stort løfte for optiske hukommelseselementerKredit:Pixabay/CC0 Public Domain Russiske kemikere har fået et nyt fotokromt kompleks bestående af vismut (III) og viologenkationer og brugt den nye forbindelse til at skabe optiske hukommelsesele
Fotokrome vismutkomplekser viser et stort løfte for optiske hukommelseselementerKredit:Pixabay/CC0 Public Domain Russiske kemikere har fået et nyt fotokromt kompleks bestående af vismut (III) og viologenkationer og brugt den nye forbindelse til at skabe optiske hukommelsesele -
 Forskere finder en måde at udnytte hele spektret af sollysForskere har vist, for første gang, at det er muligt at indsamle energi fra hele det synlige spektrum af sollys og transformere det, hurtigt og effektivt, til brint som brændstof. Kredit:David Monje p
Forskere finder en måde at udnytte hele spektret af sollysForskere har vist, for første gang, at det er muligt at indsamle energi fra hele det synlige spektrum af sollys og transformere det, hurtigt og effektivt, til brint som brændstof. Kredit:David Monje p -
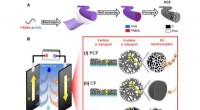 Porøse kulstof nanofibre demonstrerer exceptionel kapacitiv deioniseringSkematiske illustrationer af PCF-forberedelse og kapacitiv deionisering. (A) Syntese af PCF fra PMMA-b-PAN via elektrospinning af PMMA-b-PAN til fibre, selvsamling af PMMA-b-PAN til uordnede, bikontin
Porøse kulstof nanofibre demonstrerer exceptionel kapacitiv deioniseringSkematiske illustrationer af PCF-forberedelse og kapacitiv deionisering. (A) Syntese af PCF fra PMMA-b-PAN via elektrospinning af PMMA-b-PAN til fibre, selvsamling af PMMA-b-PAN til uordnede, bikontin -
 Scanner til malerier viser sig at være et lovende nyt CSI -værktøjFire forskellige blodpletter på en sort T-shirt, synliggjort ved hjælp af MA-XRF på basis af jern- og kaliumsignalet. Kredit:Delft University of Technology Et forskningssamarbejde har introduceret
Scanner til malerier viser sig at være et lovende nyt CSI -værktøjFire forskellige blodpletter på en sort T-shirt, synliggjort ved hjælp af MA-XRF på basis af jern- og kaliumsignalet. Kredit:Delft University of Technology Et forskningssamarbejde har introduceret
- Atacamas nattehimmelmagi
- Overfører stråling af termisk energi, når partikler bevæger sig fra et sted til et andet?
- Hvad giver energi til cellen uden at bruge ilt?
- Hvor lang tid tager det for energien fra kernen at få overflade af solen?
- Hundetelepati? Undersøgelse udforsker, hvordan hunde tænker og lærer om menneskelig adfærd
- Hvilken form for energi har en hamburger?


