Koncentrationen af iodidioner i en 0,193 m opløsningsbarium er?
De manglende oplysninger:
* Bariumforbindelsen: Spørgsmålet hedder "A 0,193 M Solution Barium." Dette er ufuldstændigt. Vi er nødt til at kende den specifikke bariumforbindelse Det er opløst i opløsningen. Eksempler kunne være:
* Bariumiodid (Bai₂)
* Bariumchlorid (bacl₂)
* Bariumnitrat (BA (no₃) ₂)
Sådan beregnes iodidkoncentration
1. Identificer bariumforbindelsen: Du har brug for disse oplysninger fra sammenhæng med problemet eller fra yderligere detaljer.
2. Skriv opløsningsligningen: For eksempel, hvis forbindelsen er bariumiodid (bai₂):
Bai₂ (S) → Ba²⁺ (aq) + 2i⁻ (aq)
3. Bestem iodidionforholdet: I dette eksempel producerer hver formelenhed af Bai₂ to iodidioner (i⁻).
4. Beregn iodidkoncentrationen:
* Hvis bariumforbindelsen er bai₂:
* Iodidkoncentrationen er to gange Bariumkoncentrationen:0,193 m Bai₂ * 2 = 0,386 m i⁻
Vigtige noter:
* Hvis forbindelsen ikke er bariumiodid, skal du justere iodidion -forholdet baseret på den kemiske formel.
* Dette antager, at bariumforbindelsen opløses helt i vand.
Fortæl mig, hvis du kan tilvejebringe den komplette bariumforbindelse, og jeg kan give dig den nøjagtige iodidkoncentration!
Sidste artikelHvad bruges alkali i?
Næste artikelHvad er specielle egenskaber ved kalsit?
 Varme artikler
Varme artikler
-
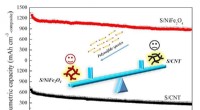 Nikkelferrit fremmer lithium-svovlbatteriets kapacitet og cyklusstabilitetSammenlignet med S/CNTer, S/NiFe2O4 har højere volumetrisk kapacitet og cykelstabilitet. Kredit:©Science China Press Lithium-svovl (Li-S) batteri kan blive praktisk, hvis 20 procent af de teoretis
Nikkelferrit fremmer lithium-svovlbatteriets kapacitet og cyklusstabilitetSammenlignet med S/CNTer, S/NiFe2O4 har højere volumetrisk kapacitet og cykelstabilitet. Kredit:©Science China Press Lithium-svovl (Li-S) batteri kan blive praktisk, hvis 20 procent af de teoretis -
 Forskere opdager nye ikke-klæbende gelerBillede af ikke-klæbende gel, der tager ved hjælp af avancerede 3D-lysmikroskopiteknikker. Kredit:University of Bristol Forskere fra University of Bristol og Université Paris-Saclay har opdaget en
Forskere opdager nye ikke-klæbende gelerBillede af ikke-klæbende gel, der tager ved hjælp af avancerede 3D-lysmikroskopiteknikker. Kredit:University of Bristol Forskere fra University of Bristol og Université Paris-Saclay har opdaget en -
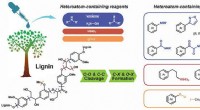 Varianter af funktionaliserede aromater ekspanderet ved heteroatom-deltaget lignin-spaltningHeteroatom-holdige reagenser udløser den katalytiske spaltning af ligninbindinger og funktionalisering af produkter samtidigt. Kredit:LI Hongji Lignin er det aromatiske polymerfragment af lignocel
Varianter af funktionaliserede aromater ekspanderet ved heteroatom-deltaget lignin-spaltningHeteroatom-holdige reagenser udløser den katalytiske spaltning af ligninbindinger og funktionalisering af produkter samtidigt. Kredit:LI Hongji Lignin er det aromatiske polymerfragment af lignocel -
 Nanokrystallinske materialer med reduceret ilt viser forbedret ydeevnePostdoktorforsker Peiman Shahbegi-Roodposhti og en bachelorstuderende i materialevidenskab arbejder med en handskekasse for at producere nanomaterialer. Kredit:University of Connecticut Forskere v
Nanokrystallinske materialer med reduceret ilt viser forbedret ydeevnePostdoktorforsker Peiman Shahbegi-Roodposhti og en bachelorstuderende i materialevidenskab arbejder med en handskekasse for at producere nanomaterialer. Kredit:University of Connecticut Forskere v
- Superladede tordenvejr:Har vi undervurderet, hvordan klimaændringer driver ekstrem regn og oversvø…
- Kan teknologigiganter arbejde sammen mod deres fælles fjender?
- Hvilken af disse er den første synlige fase måne?
- Gentagne udstrømninger af varm vind fundet tæt på sort hul
- Hvad er lipidsyntese?
- Zombier brande i Arktis ulmer under jorden og nægter at dø – hvad forårsager dem?


