Hvorfor er svovlsyre et bedre valg end ethanoisk for elektrolytten?
1. Højere ledningsevne: Svovlsyre har en signifikant højere elektrisk ledningsevne end ethansyre. Dette betyder, at det kan give mere elektrisk strøm mulighed for at strømme gennem batteriet, hvilket resulterer i bedre ydelse og effekt.
2. Større ionisering: Svovlsyre er en stærk syre, hvilket betyder, at den fuldstændigt ioniserer i opløsning og producerer en høj koncentration af brintioner (H+) og sulfationer (SO4 2-). Disse ioner er ladningsbærerne, der tillader strøm af elektricitet. Ethansyre er på den anden side en svag syre og ioniserer kun delvist, hvilket fører til lavere ledningsevne.
3. Stabilitet og levetid: Svovlsyre er mere stabil end ethansyre og nedbrydes ikke let under de barske forhold i et bilbatteri. Dette sikrer en længere levetid for batteriet og forhindrer nedbrydning af elektrolytten.
4. Nedre frysepunkt: Svovlsyre har et lavere frysepunkt end ethansyre, hvilket gør det velegnet til brug i koldere klima.
5. Lavere omkostninger: Svovlsyre er markant billigere og lettere tilgængelig end ethanesyre, hvilket gør det til et mere omkostningseffektivt valg til storstilet produktion.
Generelt gør den højere ledningsevne, større ionisering, stabilitet, lavere frysepunkt og lavere omkostninger svovlsyre til et langt overlegent valg for elektrolytten i et bilbatteri sammenlignet med ethansyre.
Sidste artikelHvordan går gas ind i en væske?
Næste artikelHvor mange atomer er der i 26,4 g Ni?
 Varme artikler
Varme artikler
-
 Registrering af forurening med en kompakt laserkildeKredit:Ecole Polytechnique Federale de Lausanne (EPFL) Forskere ved EPFL er kommet med en ny mellem infrarød lyskilde, der kan registrere drivhusgasser og andre gasser, samt molekyler i en persons
Registrering af forurening med en kompakt laserkildeKredit:Ecole Polytechnique Federale de Lausanne (EPFL) Forskere ved EPFL er kommet med en ny mellem infrarød lyskilde, der kan registrere drivhusgasser og andre gasser, samt molekyler i en persons -
 Forskere designer ny antibiofouling biomimetisk diamantfilmKredit:CC0 Public Domain Biofouling er et verdensomspændende problem, der fører til alvorlig forringelse, efter at et substrat kommer i kontakt med havvand. Traditionelle polymerer og andre antifo
Forskere designer ny antibiofouling biomimetisk diamantfilmKredit:CC0 Public Domain Biofouling er et verdensomspændende problem, der fører til alvorlig forringelse, efter at et substrat kommer i kontakt med havvand. Traditionelle polymerer og andre antifo -
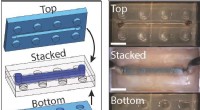 Dynamisk hydrogel bruges til at lave bløde robotkomponenter og LEGO-lignende byggeklodserLEGO-lignende hydrogel byggeklodser mønstret med bittesmå væskekanaler kan samles til komplekse mikrofluidiske enheder og derefter forsegles tæt sammen. Kredit:Wong Lab / Brown University Ved at b
Dynamisk hydrogel bruges til at lave bløde robotkomponenter og LEGO-lignende byggeklodserLEGO-lignende hydrogel byggeklodser mønstret med bittesmå væskekanaler kan samles til komplekse mikrofluidiske enheder og derefter forsegles tæt sammen. Kredit:Wong Lab / Brown University Ved at b -
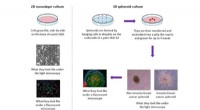 Ny indsigt i, hvordan stamceller interagerer med brystkræftceller2-D in vitro model vs 3-D in vitro model. Kredit:Dr. Morris. En Loughborough University Ph.D. studerende har givet ny indsigt i, hvordan brystkræftceller interagerer med celler i vores krop ved hj
Ny indsigt i, hvordan stamceller interagerer med brystkræftceller2-D in vitro model vs 3-D in vitro model. Kredit:Dr. Morris. En Loughborough University Ph.D. studerende har givet ny indsigt i, hvordan brystkræftceller interagerer med celler i vores krop ved hj
- Næste Mars-rover vil have 23 øjne
- Øger diffraktionen, når frekvensen stiger?
- Er Newton X Meter enheden for energi?
- Hvorfor er Supergiant Stars så lyse, selvom de ikke er særlig varme?
- Undersøgelse afslører færre skimmelsvamp toksiner i økologisk dyrket korn sammenlignet med korn …
- Krager viser avancerede indlæringsevner


