Hvor mange mol kaliumcarbonat er i 10,0 ml en 2,0 m opløsning?
1. Konverter ML til liter
* 10,0 ml * (1 l / 1000 ml) =0,010 L
2. Brug molaritetsformel
* Molaritet (m) =mol opløst / liter opløsning
* Vi kender M =2,0 m og volumen =0,010 L. Lad 'X' repræsentere molen af kaliumcarbonat.
* 2,0 m =x / 0,010 L
3. Løs for 'x' (mol kaliumcarbonat)
* x =2,0 m * 0,010 L
* x =0,020 mol
Derfor er der 0,020 mol kaliumcarbonat i 10,0 ml af en 2,0 m opløsning.
Sidste artikelHvad hedder de mindste naturlige enheder mange elementer og forbindelser?
Næste artikelHvilken syre producerer chloridsalte?
 Varme artikler
Varme artikler
-
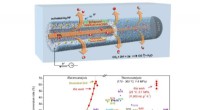 Ny sølv hulfiber booster CO2-elektroreduktionSkematisk illustration af hulfiberelektrode til at øge CO2-reduktionen til CO. Kredit:SARI Et forskerhold ledet af Profs. Wei Wei og Chen Wei fra Shanghai Advanced Research Institute (SARI) fra det
Ny sølv hulfiber booster CO2-elektroreduktionSkematisk illustration af hulfiberelektrode til at øge CO2-reduktionen til CO. Kredit:SARI Et forskerhold ledet af Profs. Wei Wei og Chen Wei fra Shanghai Advanced Research Institute (SARI) fra det -
 SMART-forskere udvikler hurtig og effektiv metode til at producere røde blodlegemerLaboratorieopsætning af mikrofluidisk sortering og oprensning af celler under dyrkning og fremstilling af røde blodlegemer. Kredit:Singapore-MIT Alliance for Research and Technology (SMART) Forske
SMART-forskere udvikler hurtig og effektiv metode til at producere røde blodlegemerLaboratorieopsætning af mikrofluidisk sortering og oprensning af celler under dyrkning og fremstilling af røde blodlegemer. Kredit:Singapore-MIT Alliance for Research and Technology (SMART) Forske -
 Forskere udvikler cellesugende teknologiPrikker i Histogram Feature Quantities svarer til hver celle. Vælg og klik på prikkerne på histogrammet for at bestemme, hvilke celler der skal suges. T baseret på de forudindstillede funktionsmængder
Forskere udvikler cellesugende teknologiPrikker i Histogram Feature Quantities svarer til hver celle. Vælg og klik på prikkerne på histogrammet for at bestemme, hvilke celler der skal suges. T baseret på de forudindstillede funktionsmængder -
 Halogenbindingsmedieret metalfri kontrolleret kationisk polymerisationGennem den reversible C-X-binding spaltning af den ioniske organokatalysator med halogenbindingsegenskaben, den metalfrie og præcisionskationiske polymerisation af vinylether fortsatte med at give pol
Halogenbindingsmedieret metalfri kontrolleret kationisk polymerisationGennem den reversible C-X-binding spaltning af den ioniske organokatalysator med halogenbindingsegenskaben, den metalfrie og præcisionskationiske polymerisation af vinylether fortsatte med at give pol


