Hvilket element er stabilt med 2 valenselektroner?
Her er hvorfor:
* Valenselektroner: Dette er elektronerne i den yderste skal af et atom, der er involveret i kemisk binding.
* stabilitet: Atomer stræber efter at opnå en stabil elektronkonfiguration, der ofte ligner den nærmeste ædle gas.
* beryllium: Beryllium har et atomnummer på 4, hvilket betyder, at det har 4 elektroner. Dens elektronkonfiguration er 1S² 2S². 2S² repræsenterer dens to valenselektroner.
* ædle gaskonfiguration: Helium (HE), den nærmeste ædle gas til beryllium, har også 2 elektroner (1S²).
Derfor skaber Berylliums to valenselektroner en stabil, ædel gaslignende konfiguration, hvilket gør den relativt ureaktiv.
 Varme artikler
Varme artikler
-
 Et termisk styringsmateriale, der reagerer på varme eller kulde ved at folde eller folde ud uden be…Inspireret af Mimosa pudica-blade vælger enheden intelligent den rigtige termiske styringstilstand ved at modulere dens morfologi. Kredit:Quan Zhang Et team af forskere ved Nankai University har ud
Et termisk styringsmateriale, der reagerer på varme eller kulde ved at folde eller folde ud uden be…Inspireret af Mimosa pudica-blade vælger enheden intelligent den rigtige termiske styringstilstand ved at modulere dens morfologi. Kredit:Quan Zhang Et team af forskere ved Nankai University har ud -
 Ny generation af kuldioxidgasseparationssystem ved hjælp af adsorbenter af gate-typeForskere i Japan har designet et adsorberende tårnsystem af gate-type, der opfanger og adskiller blandede gasser, CO2, for at muliggøre sænkning af drivhusgasemissioner fra industrielle kilder. Kredit
Ny generation af kuldioxidgasseparationssystem ved hjælp af adsorbenter af gate-typeForskere i Japan har designet et adsorberende tårnsystem af gate-type, der opfanger og adskiller blandede gasser, CO2, for at muliggøre sænkning af drivhusgasemissioner fra industrielle kilder. Kredit -
 En ny måde at fjerne generende ioner fra vandKredit:Wageningen Universitet At omdanne havvand til ferskvand er vigtigt i lande med knaphed på vand. Til den proces, visse ladede partikler - kendt som ioner - skal fjernes fra vandet. Imidlerti
En ny måde at fjerne generende ioner fra vandKredit:Wageningen Universitet At omdanne havvand til ferskvand er vigtigt i lande med knaphed på vand. Til den proces, visse ladede partikler - kendt som ioner - skal fjernes fra vandet. Imidlerti -
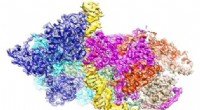 Højopløsningsbillede af strukturen af oprindelsesgenkendelseskomplekset bundet til DNA afsløretSide- (Orc1/2) og bundbillede (WHD) af ORC-DNA-komplekset (72-bp). Kredit:Division of Life Science, Hong Kong University of Science and Technology Celler formerer sig ved at lave kopier af sig sel
Højopløsningsbillede af strukturen af oprindelsesgenkendelseskomplekset bundet til DNA afsløretSide- (Orc1/2) og bundbillede (WHD) af ORC-DNA-komplekset (72-bp). Kredit:Division of Life Science, Hong Kong University of Science and Technology Celler formerer sig ved at lave kopier af sig sel


