PH -værdi på 50 cm3 0,1moldm3 saltsyreblanding med 100 0,05 MoldM3 natriumhydroxid?
1. Beregn molen af HCL og NaOH:
* mol HCL: (0,1 mol/dm³) * (50 cm³/1000 cm³/dm³) =0,005 mol
* mol NaOH: (0,05 mol/dm³) * (100 cm³/1000 cm³/dm³) =0,005 mol
2. Bestem den begrænsende reaktant:
* HCL og NaOH reagerer i et forhold på 1:1. Da vi har lige mol af begge dele, vil de neutralisere hinanden fuldstændigt.
3. Beregn koncentrationen af overskydende reaktant (som ikke er nogen i dette tilfælde):
* Da reaktionen er afsluttet, er der ingen overskydende HCL eller NaOH tilbage.
4. Beregn pH:
* Løsningen vil være neutral, fordi al syre og base har reageret.
* PH for en neutral opløsning er 7 .
Derfor er blandingen af blandingen 7.
 Varme artikler
Varme artikler
-
 CO2-neutral brint fra biomasseKredit:Vienna University of Technology Uden fossile brændstoffer, der kan ikke være nogen højovnsproces – men brint kan spille en vigtigere rolle i fremtiden. En miljøvenlig proces er ved at blive
CO2-neutral brint fra biomasseKredit:Vienna University of Technology Uden fossile brændstoffer, der kan ikke være nogen højovnsproces – men brint kan spille en vigtigere rolle i fremtiden. En miljøvenlig proces er ved at blive -
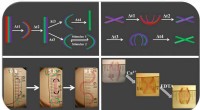
 Tidlig sygdomsdiagnose kan forbedres dramatisk med nyt detektionssystemKredit:Imperial College London Ved at knytte specialiserede molekyler til rygraden af DNA, forskere har gjort det lettere at opdage sjældne molekyler forbundet med tidlig sygdom. Tilstedeværels
Tidlig sygdomsdiagnose kan forbedres dramatisk med nyt detektionssystemKredit:Imperial College London Ved at knytte specialiserede molekyler til rygraden af DNA, forskere har gjort det lettere at opdage sjældne molekyler forbundet med tidlig sygdom. Tilstedeværels -
 Forskerteam viser komplekse, 3D-printede schwarzitter modstår tryk, når de er belagtEn komprimeringstest af 3D-printede schwarzitter, der enten er belagt eller ikke-belagt med en tynd polymer, viser, hvordan polymeren holder keramikken i stykker. Materialerne kan bruges hvor som hels
Forskerteam viser komplekse, 3D-printede schwarzitter modstår tryk, når de er belagtEn komprimeringstest af 3D-printede schwarzitter, der enten er belagt eller ikke-belagt med en tynd polymer, viser, hvordan polymeren holder keramikken i stykker. Materialerne kan bruges hvor som hels -
 4-D bioingeniørmaterialer bøjning, kurve som naturligt væv4D hydrogel-baserede materialer kan gennemgå flere konformationelle formændringer som reaktion på miljømæssige signaler. Kredit:Aixiang Ding Vævsteknik har længe været afhængig af geometrisk stati
4-D bioingeniørmaterialer bøjning, kurve som naturligt væv4D hydrogel-baserede materialer kan gennemgå flere konformationelle formændringer som reaktion på miljømæssige signaler. Kredit:Aixiang Ding Vævsteknik har længe været afhængig af geometrisk stati
- New Horizons returnerer sidste bit af 2015 flyby-data til Jorden
- Hvad er 4 ressourcer leveret af et levested?
- Hvilken tilstand af stof har mindst partikler i et givet volumen?
- Hvordan får du strøm ind i din månebase? Med et flere kilometer højt tårn af beton
- Hvad er et solidt stof, der findes i naturen, som uorganisk?
- Dyrkning af kulstof nanorør med det rigtige twist


