Hvilke atomer vil have de samme kemiske egenskaber som calcium?
Calcium (CA) er i gruppe 2 , også kendt som alkaliske jordmetaller . Derfor vil andre alkaliske jordmetaller have lignende kemiske egenskaber. Disse inkluderer:
* beryllium (BE)
* magnesium (mg)
* strontium (SR)
* barium (BA)
* radium (RA)
Hvorfor har de lignende egenskaber:
Alle disse elementer har to valenselektroner. Dette betyder, at de har en tendens til at miste disse to elektroner til at danne en +2 -kation, og derfor er de alle reaktive metaller. De deler også lignende reaktivitetsmønstre og danner lignende typer forbindelser.
Det er dog vigtigt at bemærke, at der vil være nogle forskelle i reaktivitet på grund af deres forskellige atomstørrelser og ioniseringsenergier. For eksempel er calcium mere reaktiv end magnesium, og barium er mere reaktiv end calcium.
Sidste artikelHvor mange kloratomer er der i forbindelseskaliumchloratet?
Næste artikelHvad er den første ioniseringsenergi af svovl?
 Varme artikler
Varme artikler
-
 Bæredygtigt byggeri ved hjælp af miljøvenlig betonForskellige former testet for den smeltbare metalfiber. Kredit:Tokyo Institute of Technology Den 18. februar Lektor Masatoshi Kondo (Laboratory for Advanced Nuclear Energy, Institut for Innovativ
Bæredygtigt byggeri ved hjælp af miljøvenlig betonForskellige former testet for den smeltbare metalfiber. Kredit:Tokyo Institute of Technology Den 18. februar Lektor Masatoshi Kondo (Laboratory for Advanced Nuclear Energy, Institut for Innovativ -
 Forskere udvikler en ny heterostrukturkatalysator til effektiv brintgenerering fra vandspaltningAC Transit brint brændselscelle bus. Kredit:Eric Fischer. Bekymringer om stigende atmosfæriske kuldioxidniveauer og global opvarmning har gjort det til en miljømæssig nødvendighed at erstatte fossi
Forskere udvikler en ny heterostrukturkatalysator til effektiv brintgenerering fra vandspaltningAC Transit brint brændselscelle bus. Kredit:Eric Fischer. Bekymringer om stigende atmosfæriske kuldioxidniveauer og global opvarmning har gjort det til en miljømæssig nødvendighed at erstatte fossi -
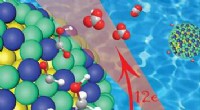 Ny kerne-skal katalysator til ethanol brændselscellerEt nærbillede af platin/iridium (grøn/blå) skallen over en guld nanopartikelkerne (gul), viser, hvordan denne katalysator spalter carbon-carbon (grå) bindingerne i ethanol, mens den oprindeligt efterl
Ny kerne-skal katalysator til ethanol brændselscellerEt nærbillede af platin/iridium (grøn/blå) skallen over en guld nanopartikelkerne (gul), viser, hvordan denne katalysator spalter carbon-carbon (grå) bindingerne i ethanol, mens den oprindeligt efterl -
 Undersøgelse skyller hudenKAUST-forskere har brugt komplementære teknikker til at adskille rent grænsefladeeffekter fra elektrospray-specifikke effekter. Kredit:Ivan Gromicho Fra den vindpiskede overflade af det åbne hav,
Undersøgelse skyller hudenKAUST-forskere har brugt komplementære teknikker til at adskille rent grænsefladeeffekter fra elektrospray-specifikke effekter. Kredit:Ivan Gromicho Fra den vindpiskede overflade af det åbne hav,
- Forskning:Et lands grad af ligestilling mellem kønnene kan påvirke mænds evne til at genkende ber…
- Hvad er 50 nanogrammer?
- Problem med nøglespildstørrelse:Hvor meget og betyder det noget?
- Tidoblet stigning i nedskæringer i CO2-emissioner, der er nødvendige for at dæmme op for klimakri…
- Hvilken organisk forbindelse giver cellen energi?
- NASA, NOAA-satellitter viser vindforskydning, der påvirker den tropiske storm Ida


