Hvordan kan der dannes en kovalent binding mellem hydrogenatom og kloratom?
forståelse af det grundlæggende
* brint (H): Har 1 Proton og 1 elektron. Det har brug for 1 mere elektron for at opnå en stabil, fuld ydre skal.
* klor (Cl): Har 17 protoner og 17 elektroner. Det har brug for 1 mere elektron for at opnå en stabil, fuld ydre skal.
den kovalente bindingsdannelse
1. Deling af elektroner: Hydrogen og klor har hver en elektron i deres yderste skal. For at blive stabile deler de disse elektroner. Dette delte par elektroner tæller nu mod begge atomernes ydre skaller, hvilket gør hvert atom effektivt har en fuld ydre skal.
2. Dannelse af molekylet: Det delte elektronpar skaber en stærk attraktion mellem brint- og chloratomer, der danner en kovalent binding. Denne binding er repræsenteret af en enkelt linje i en strukturel formel (H-CL).
3. Polaritet: Mens obligationen er kovalent, er den ikke perfekt ens. Klor er meget mere elektronegativ end brint, hvilket betyder, at det tiltrækker de delte elektroner stærkere. Dette skaber en delvis negativ ladning (Δ-) på chloratomet og en delvis positiv ladning (Δ+) på hydrogenatomet. Dette gør H-CL-bindingen til en polær kovalent binding.
resume
Den kovalente binding mellem brint og klor dannes ved deling af elektroner, hvilket skaber et stabilt molekyle af brintchlorid (HCI), også kendt som saltsyre. Delingen er ikke perfekt ens, hvilket fører til en polær binding.
Sidste artikelHvor mange elektroner deler carbon for at afslutte sin valensskal?
Næste artikelHvilken type ligand er nitrogendioxid?
 Varme artikler
Varme artikler
-
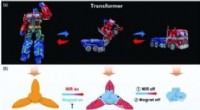 Magnetisk styret, hydrogelbaserede smarte transformerea) Billeder, der viser en transformers formtransformation. b) Formtransformationsprocessen for en blød hydrogeltransformator under koblingen af magnetfelt og NIR. c) SEM -billederne af HG -Fe3O4 -hy
Magnetisk styret, hydrogelbaserede smarte transformerea) Billeder, der viser en transformers formtransformation. b) Formtransformationsprocessen for en blød hydrogeltransformator under koblingen af magnetfelt og NIR. c) SEM -billederne af HG -Fe3O4 -hy -
 Båndets historie:Klæbrige bits gør bedre batterierTil venstre, en kobberstrømsamler med en laserinduceret siliciumoxidbelægning skabt på Rice University. Til højre, et scanningselektronmikroskopbillede af belægningen skabt ved lasning af tape på kobb
Båndets historie:Klæbrige bits gør bedre batterierTil venstre, en kobberstrømsamler med en laserinduceret siliciumoxidbelægning skabt på Rice University. Til højre, et scanningselektronmikroskopbillede af belægningen skabt ved lasning af tape på kobb -
 Et molekyle, der fungerer som et nanobatteriHPC-klyngen CARL hjalp med at dechifrere molekylets adfærd gennem omfattende beregninger. Kredit:Daniel Schmidt/University of Oldenburg Hvordan fungerer molekylære katalysatorer - molekyler, som s
Et molekyle, der fungerer som et nanobatteriHPC-klyngen CARL hjalp med at dechifrere molekylets adfærd gennem omfattende beregninger. Kredit:Daniel Schmidt/University of Oldenburg Hvordan fungerer molekylære katalysatorer - molekyler, som s -
 3D-udskrivning af den første biomimetiske tungeoverflade nogensindeDen 3D -printede negative form viser huller til filiforme og fungiforme papiller. Kredit:University of Leeds Forskere har skabt syntetiske bløde overflader med tungelignende teksturer for første g
3D-udskrivning af den første biomimetiske tungeoverflade nogensindeDen 3D -printede negative form viser huller til filiforme og fungiforme papiller. Kredit:University of Leeds Forskere har skabt syntetiske bløde overflader med tungelignende teksturer for første g
- Tror du, at chimpansesenge er mere beskidte end menneskelige? igen
- Hvilke kræfter har formet overflade over millioner af år?
- Kan kunstig intelligens hjælpe med at forhindre selvmord?
- Potentiel toksicitet af cellulosenanokrystaller undersøgt
- Ultrahurtig og koblet:Atomiske vibrationer i kvantematerialet bornitrid
- Stærk cyklon slår østindien, påvirker det asiatiske subkontinent


