Kan et kloratom kun danne en ionisk binding?
* ioniske bindinger: Klor danner typisk en ionisk binding på grund af dens høje elektronegativitet. Det får en elektron for at opnå en stabil oktetkonfiguration, der danner en -1 -ladning (CL⁻). Denne ioniske binding dannes med et metalatom, der mister en elektron.
* kovalente obligationer: Klor kan også danne kovalente bindinger og dele elektroner med andre ikke -metale atomer. Det kan danne en, to eller endda tre kovalente obligationer . For eksempel:
* hcl: Klor danner en enkelt kovalent binding med brint.
* cl₂: Klor danner en enkelt kovalent binding med et andet kloratom.
* clo₂: Klor danner to kovalente bindinger med iltatomer.
Kortfattet: Klor kan danne forskellige typer bindinger afhængigt af det andet involverede atom. Den danner typisk en ionisk binding, men den kan også danne flere kovalente bindinger.
Sidste artikelHvad er fluormasse nummer?
Næste artikelHvad er den kemiske formel for hydrogenperoxid plus kaliumiodid?
 Varme artikler
Varme artikler
-
 Team -afkodet molekylær mekanisme, der hæmmer sværmende motilitet hos bakteriepopulationerDr. Thomas Boettcher. Kredit:University of Konstanz I naturen, bakterier forekommer mest i multicellulære kollektiver, frem for som enkeltpersoner. De er i stand til at koordinere deres adfærd, me
Team -afkodet molekylær mekanisme, der hæmmer sværmende motilitet hos bakteriepopulationerDr. Thomas Boettcher. Kredit:University of Konstanz I naturen, bakterier forekommer mest i multicellulære kollektiver, frem for som enkeltpersoner. De er i stand til at koordinere deres adfærd, me -
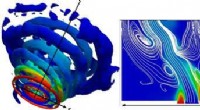 Minimering af ammoniak -brændstofemissionerTil venstre:Vortex strukturer af hvirvlende strømme. Til højre:Blanding af mønster af to ammoniakstrømme med luftstrømmen nær hvirvlerne, placeret i bunden af figuren. Farver angiver fordeling af am
Minimering af ammoniak -brændstofemissionerTil venstre:Vortex strukturer af hvirvlende strømme. Til højre:Blanding af mønster af to ammoniakstrømme med luftstrømmen nær hvirvlerne, placeret i bunden af figuren. Farver angiver fordeling af am -
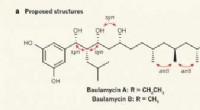 Kemikere udleder den korrekte struktur af A- og B-baulamycinerneTidligere foreslåede og faktiske molekylære strukturer af baulamycinerne. Kredit: Natur (2017). doi:10.1038/nature23265 (Phys.org) – Et team af kemikere ved University of Bristol har korrekt udle
Kemikere udleder den korrekte struktur af A- og B-baulamycinerneTidligere foreslåede og faktiske molekylære strukturer af baulamycinerne. Kredit: Natur (2017). doi:10.1038/nature23265 (Phys.org) – Et team af kemikere ved University of Bristol har korrekt udle -
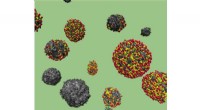 Syntesestudier omdanner affaldssukker til bæredygtige energilagringsapplikationerEn molekylær dynamik-simulering afbilder solide (sort) og hule (flerfarvede) kulstofkugler afledt af affaldssukkerstrømme fra bioraffinaderier. De hule kuglers egenskaber er ideelle til udvikling af e
Syntesestudier omdanner affaldssukker til bæredygtige energilagringsapplikationerEn molekylær dynamik-simulering afbilder solide (sort) og hule (flerfarvede) kulstofkugler afledt af affaldssukkerstrømme fra bioraffinaderier. De hule kuglers egenskaber er ideelle til udvikling af e
- Hvilken lovtilstand er afhængig af massen og accelerationen af et objekt?
- Hvad kaldes processen, når syrer og baser reagerer og danner saltvand?
- Er en energibesparende trust penge?
- Ny grafitbaseret hurtig sensorchip til teofyllinovervågning i realtid
- Lasersmeltning:Færre ukendte i lasernanosyntesen af kompositter
- Hvorfor ville opvarmning af gassen i luftballonen stige?


