Hvor mange natriumioner er der i 25,75 gram chlorid?
1. Forstå den kemiske formel
Natriumchlorid (NaCl) har et forhold på 1:1 af natrium (Na+) ioner til chlorid (Cl-) -ioner. Dette betyder for hver chloridion, der er en natriumion.
2. Beregn mol chlorid
* Find den molære masse af chlorid (CL): Den molære masse af klor er 35,45 g/mol.
* Del massen af chlorid med dets molære masse:
25,75 g Cl / 35,45 g / mol Cl =0,727 mol Cl
3. Beregn mol af natrium
* Brug molforholdet fra den kemiske formel: Da der er en natriumion for hver chloridion, er der også 0,727 mol natriumioner.
4. Beregn antallet af natriumioner
* Brug Avogadros nummer: 6,022 x 10^23 ioner/mol
* Multiplicer molen af natrium med Avogadro's nummer: 0,727 mol Na x 6,022 x 10^23 ioner/mol =4,38 x 10^23 natriumioner
Derfor er der ca. 4,38 x 10^23 natriumioner i 25,75 gram chlorid.
 Varme artikler
Varme artikler
-
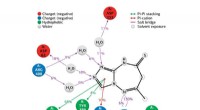 Chemist syntetiserer nye forbindelser med stærke antidiabetiske egenskaberKredit:RUDN Universitet En kemiker fra RUDN University har syntetiseret nye derivater af 1, 2, 4-triazol, der udviser antidiabetiske egenskaber. Eksperimenter viste, at disse forbindelser virker b
Chemist syntetiserer nye forbindelser med stærke antidiabetiske egenskaberKredit:RUDN Universitet En kemiker fra RUDN University har syntetiseret nye derivater af 1, 2, 4-triazol, der udviser antidiabetiske egenskaber. Eksperimenter viste, at disse forbindelser virker b -
 Lokalisering af d-orbitale elektroner i overgangsmetaller bestemtL3 og L2 fotoelektron L2,3 VV Auger-elektronsammenfaldskort af Cu (a) og Co (b) sammen med det sammenfaldende fotoelektronspektrum opnået ved integration af kortene langs Auger-elektronens kinetiske
Lokalisering af d-orbitale elektroner i overgangsmetaller bestemtL3 og L2 fotoelektron L2,3 VV Auger-elektronsammenfaldskort af Cu (a) og Co (b) sammen med det sammenfaldende fotoelektronspektrum opnået ved integration af kortene langs Auger-elektronens kinetiske -
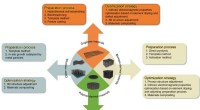 Seneste fremskridt inden for tredimensionelle porøse kulstofmaterialer til elektromagnetisk bølgea…Forskellige forberedelsesprocesser og optimeringsstrategier for 3D carbon EWAMer er opsummeret her. Kredit:Science China Press For nylig offentliggjorde professor Jiurong Liu og professor Zhihui Ze
Seneste fremskridt inden for tredimensionelle porøse kulstofmaterialer til elektromagnetisk bølgea…Forskellige forberedelsesprocesser og optimeringsstrategier for 3D carbon EWAMer er opsummeret her. Kredit:Science China Press For nylig offentliggjorde professor Jiurong Liu og professor Zhihui Ze -
 Forskere afslører robust ethan-fangende porøst organisk bur til effektiv anvendelse af ethylenrens…Kredit:Prof. YUANs gruppe Fjernelse af ethan (C 2 H 6 ) fra dets analoge ethylen (C 2 H 4 ) er af stor betydning i den petrokemiske industri, og er meget udfordrende på grund af deres lign
Forskere afslører robust ethan-fangende porøst organisk bur til effektiv anvendelse af ethylenrens…Kredit:Prof. YUANs gruppe Fjernelse af ethan (C 2 H 6 ) fra dets analoge ethylen (C 2 H 4 ) er af stor betydning i den petrokemiske industri, og er meget udfordrende på grund af deres lign
- Udformning af, hvordan deformerbarhed af røde blodlegemer vurderes - forskere udvikler en ny tilgan…
- Hvad hedder de vulkanske landformer ved divergerende havpladegrænser?
- Tilpasning af havplanter
- Forældre siger, at deres børn har undervisere til at udfylde huller, ikke at oplade forud
- Hvad er de tre vigtigste anvendelser af kalksten?
- Når et objekt bevæger sig rundt om den cirkulære sporcentripetalkraft leveres af?


