Hvad er mængden af H2O -molekyler i 20G CUSO4.5H2O?
1. Find den molære masse af CUSO4.5H2O:
* CU:63,55 g/mol
* S:32,06 g/mol
* O (i CUSO4):4 * 16,00 g/mol =64,00 g/mol
* H2O:5 * (2 * 1,01 + 16,00) G/mol =90,05 g/mol
Samlet molmasse CUSO4,5H2O =63,55 + 32,06 + 64,00 + 90,05 = 249,66 g/mol
2. Beregn molen af CUSO4.5H2O:
* Mol =masse / molær masse
* Mol =20 g / 249,66 g / mol =0,0801 mol
3. Bestem molen af vandmolekyler:
* Da der er 5 mol vandmolekyler for hver 1 mol CUSO4,5H2O, har vi:
* Mol H2O =0,0801 mol CUSO4,5H2O * (5 mol H2O / 1 mol CUSO4,5H2O) =0,4005 mol H2O
4. Konverter mol vand til antal molekyler:
* Avogadros nummer:6,022 x 10^23 molekyler/mol
* Antal H2O -molekyler =0,4005 mol * (6,022 x 10^23 molekyler/mol) = 2,41 x 10^23 molekyler
Derfor er der ca. 2,41 x 10^23 vandmolekyler i 20 g CUSO4,5H2O.
Sidste artikelHvad er forskellen mellem oxid og dioxid?
Næste artikelHvad er forskellen i et rent stof og en blanding?
 Varme artikler
Varme artikler
-
 Detaljeret billede afslører, hvordan tandemaljen er stærk nok til at holde livet udPIC -kortlægning, som måler biominerale krystalorienteringer og tildeler forskellige farver til forskellige rotationsvinkler, afslører, at krystallerne i tandemaljen ikke er perfekt justeret. Kredit:P
Detaljeret billede afslører, hvordan tandemaljen er stærk nok til at holde livet udPIC -kortlægning, som måler biominerale krystalorienteringer og tildeler forskellige farver til forskellige rotationsvinkler, afslører, at krystallerne i tandemaljen ikke er perfekt justeret. Kredit:P -
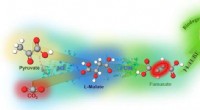 Lektioner fra naturlig fotosyntese til omdannelse af CO2 til råmaterialer til plastFumarat syntetiseres ved at binde CO2 til pyruvat med multi-biokatalysatorer. Malatdehydrogenase (ME) kombinerer pyruvat og kuldioxid (CO2) til L-malat, som kan omdannes til fumarat af fumarase (FUM).
Lektioner fra naturlig fotosyntese til omdannelse af CO2 til råmaterialer til plastFumarat syntetiseres ved at binde CO2 til pyruvat med multi-biokatalysatorer. Malatdehydrogenase (ME) kombinerer pyruvat og kuldioxid (CO2) til L-malat, som kan omdannes til fumarat af fumarase (FUM). -
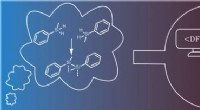 Forskere først til at forbinde silicium atomer på overfladerSkematisk repræsentation af de involverede discipliner (i midten) og transformationen af ideen (venstre) til det endelige produkt (højre). I baggrunden til højre er et scanning tunneling mikroskop b
Forskere først til at forbinde silicium atomer på overfladerSkematisk repræsentation af de involverede discipliner (i midten) og transformationen af ideen (venstre) til det endelige produkt (højre). I baggrunden til højre er et scanning tunneling mikroskop b -
 Video:Coronavirus-vaccine:Hvor er vi, og hvad er det næste?Kredit:The American Chemical Society Du har måske hørt, at COVID-19-vaccineforsøg er i gang i Seattle. Hvad er det præcist, der testes? Hvor meget længere vil disse test tage? Og hvornår kan vi f
Video:Coronavirus-vaccine:Hvor er vi, og hvad er det næste?Kredit:The American Chemical Society Du har måske hørt, at COVID-19-vaccineforsøg er i gang i Seattle. Hvad er det præcist, der testes? Hvor meget længere vil disse test tage? Og hvornår kan vi f


