Hvor mange gram bariumbromid BABR2 er til stede i 3,56 mol denne forbindelse?
1. Find den molære masse af babr₂:
* Barium (BA) har en molmasse på 137,33 g/mol
* Brom (BR) har en molmasse på 79,90 g/mol
* Da der er to bromatomer, er den samlede masse af brom 2 * 79,90 g/mol =159,80 g/mol
* Den molære masse af Babr₂ er 137,33 g/mol + 159,80 g/mol =297,13 g/mol
2. Brug den molære masse til at konvertere mol til gram:
* Gram =mol * molmasse
* Gram =3,56 mol * 297,13 g/mol
* Gram ≈ 1058,6 g
Derfor er ca. 1058,6 gram bariumbromid til stede i 3,56 mol af forbindelsen.
Sidste artikelHvorfor nitrogen er gas, men fosfor er et fast stof?
Næste artikelHvilke ændringer i farve, når brom reagerer med en alkyne?
 Varme artikler
Varme artikler
-
 Uden for vægten:Fiskepanser både sejt og fleksibeltOptisk mikroskopibillede af tværsnittet af en karpeskala, der viser en flerlagsstruktur. Kredit:Quan et al., Struktur og mekanisk tilpasningsevne af en moderne Elasmoid fiskeskala fra almindelig karpe
Uden for vægten:Fiskepanser både sejt og fleksibeltOptisk mikroskopibillede af tværsnittet af en karpeskala, der viser en flerlagsstruktur. Kredit:Quan et al., Struktur og mekanisk tilpasningsevne af en moderne Elasmoid fiskeskala fra almindelig karpe -
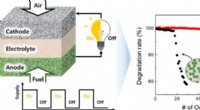 Reduceret nikkelindhold og forbedret stabilitet og ydeevne i keramiske brændselscellerKonceptuelt diagram over oxidations-reduktionscyklus af keramiske brændselsceller og sammenligning af nyt koncept vs. forringelsesrate for konventionelle brændstofplader Kredit:Korea Institute of Scie
Reduceret nikkelindhold og forbedret stabilitet og ydeevne i keramiske brændselscellerKonceptuelt diagram over oxidations-reduktionscyklus af keramiske brændselsceller og sammenligning af nyt koncept vs. forringelsesrate for konventionelle brændstofplader Kredit:Korea Institute of Scie -
 Forskere rydder bane for tinbaserede perovskit-solcellerKredit:CC0 Public Domain Forskere ved University of Surrey mener, at deres tinbaserede perovskit-solcelle kan rydde banen for solpanelteknologi til at tage fart og hjælpe Storbritannien med at nå
Forskere rydder bane for tinbaserede perovskit-solcellerKredit:CC0 Public Domain Forskere ved University of Surrey mener, at deres tinbaserede perovskit-solcelle kan rydde banen for solpanelteknologi til at tage fart og hjælpe Storbritannien med at nå -
 En unik ledende tilstand under UV-bestrålingEt skud UV-lys har produceret en betydelig strøm af elektrisk strøm som kildevand i en isolerende molekylær krystal, hvilket fænomen stammer fra dette materiales unikke oprindelige fysiske egenskaber,
En unik ledende tilstand under UV-bestrålingEt skud UV-lys har produceret en betydelig strøm af elektrisk strøm som kildevand i en isolerende molekylær krystal, hvilket fænomen stammer fra dette materiales unikke oprindelige fysiske egenskaber,
- Hvorfor er månen ikke-luminøs, selvom den afgiver lys?
- Hvem for første gang bestemte med succes afgift for en elektron?
- NASA-NOAA-satellitten ser på den storøjede tropiske cyklon Oma
- Hvordan at lytte efter den rigtige buzz forhindrer myg i at parre sig med forkerte arter
- Kan genterapi kurere skaldethed?
- Hvilken type sten danner dybest inde i Jorden?


