Hvad er molfraktionen af opløst stof i en 3,71 m vandig opløsning?
Forståelse af molalitet
* molalitet (m) er et mål for koncentration defineret som antallet af mol opløst stof pr. Kg opløsningsmiddel.
* I dette tilfælde har vi en 3,71 m opløsning, hvilket betyder, at der er 3,71 mol opløst stof for hvert 1 kg vand (opløsningsmidlet).
Beregning af molfraktion
Molfraktionen af en komponent (opløst eller opløsningsmiddel) er forholdet mellem antallet af mol af denne komponent og det samlede antal mol i opløsningen.
1. mol opløsningsmiddel:
* Da vi har 1 kg vand, og den molære vandmasse er 18,015 g/mol, kan vi beregne vandmolene:
* Mol vand =(1000 g) / (18,015 g / mol) =55,51 mol
2. Samlede mol:
* Samlet mol i opløsningen =mol af opløst stof + mol vand
* Samlet mol =3,71 mol + 55,51 mol =59,22 mol
3. molfraktion af opløst stof:
* Molfraktion af opløst
* X_solute =3,71 mol / 59,22 mol = 0,0626
Derfor er molfraktionen af opløsningen i en 3,71 m vandig opløsning 0,0626.
Sidste artikelHvilken forbindelse fremstiller aluminiumsbrom og ilt?
Næste artikelHvorfor er natriumhydroxid velegnet til absorberende brom?
 Varme artikler
Varme artikler
-
 Et nyt kig på farvedisplaysMagnus Jonsson, lektor, og Shangzhi Chen, postdoc, ved Laboratory of Organic Electronics ved Linköpings Universitet. Kredit:Thor Balkhed Forskere ved Linköpings Universitet har udviklet en metode,
Et nyt kig på farvedisplaysMagnus Jonsson, lektor, og Shangzhi Chen, postdoc, ved Laboratory of Organic Electronics ved Linköpings Universitet. Kredit:Thor Balkhed Forskere ved Linköpings Universitet har udviklet en metode, -
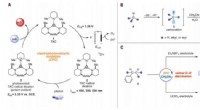 Elektrofotokatalytisk diamination af vicinale C -H -bindingerElektrofotokatalytisk amination af C -H -bindinger. (A) Generisk elektrofotokatalytisk cyklus med trisaminocyclopropenium (TAC) 1. (B) Ritter-type C-H amineringsreaktion. (C) Elektrofotokatalytiske vi
Elektrofotokatalytisk diamination af vicinale C -H -bindingerElektrofotokatalytisk amination af C -H -bindinger. (A) Generisk elektrofotokatalytisk cyklus med trisaminocyclopropenium (TAC) 1. (B) Ritter-type C-H amineringsreaktion. (C) Elektrofotokatalytiske vi -
 Rumtemperaturkonvertering af CO2 til CO:En ny måde at syntetisere kulbrinter påIllustration af en ny stuetemperaturproces til fjernelse af kuldioxid (CO 2 ) ved at omdanne molekylet til kulilte (CO). I stedet for at bruge varme, nanoskalametoden er afhængig af energien fra ove
Rumtemperaturkonvertering af CO2 til CO:En ny måde at syntetisere kulbrinter påIllustration af en ny stuetemperaturproces til fjernelse af kuldioxid (CO 2 ) ved at omdanne molekylet til kulilte (CO). I stedet for at bruge varme, nanoskalametoden er afhængig af energien fra ove -
 Frigør perovskites potentiale for solcellerSolceller lavet af perovskit lover meget, dels fordi de nemt kan laves på fleksible underlag, som denne eksperimentelle celle. Kredit:Ken Richardson Perovskites - en bred kategori af forbindelser,
Frigør perovskites potentiale for solcellerSolceller lavet af perovskit lover meget, dels fordi de nemt kan laves på fleksible underlag, som denne eksperimentelle celle. Kredit:Ken Richardson Perovskites - en bred kategori af forbindelser,
- Udfordringer i udviklingen af elektrokatalysatorer
- Påvirker størrelsen på en raket dens hastighed?
- Hvordan påvirker Coriolis -virkningen overfladestrømme?
- Hvor mange inches er 0,35 cm?
- Hvad ville der ske, hvis gasser absorberer synligt lys?
- Hjælper dekonstruktive kræfter som erosion med at opbygge jordoverfladen?


