Hvad er masseprocenten af H i ammoniumbicarbonat?
1. Find den molære masse af ammoniumbicarbonat:
* N:14,01 g/mol
* H:1,01 g/mol (x 5) =5,05 g/mol
* C:12,01 g/mol
* O:16,00 g/mol (x 3) =48,00 g/mol
Samlet molmasse =14,01 + 5,05 + 12,01 + 48,00 = 79,07 g/mol
2. Beregn massen af brint i en mol ammoniumbicarbonat:
* Masse af H =5,05 g/mol
3. Beregn masseprocenten af brint:
* Masseprocent af h =(masse af h / molmasse af nh₄hco₃) x 100%
* Masseprocent af h =(5,05 g/mol/79,07 g/mol) x 100%
* Masseprocent af H =6,39%
Derfor er masseprocenten af brint i ammoniumbicarbonat ca. 6,39%.
Sidste artikelNatrium eller jern er mere reaktiv?
Næste artikelHvor mange iltatomer er til stede i 5,2 g 02?
 Varme artikler
Varme artikler
-
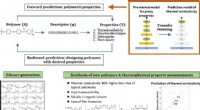 Succesfuld anvendelse af maskinlæring i opdagelsen af nye polymererKredit:Tokyo Tech En fælles forskergruppe, herunder Ryo Yoshida (professor og direktør for Data Science Center for Creative Design and Manufacturing ved Institute of Statistical Mathematics [ISM],
Succesfuld anvendelse af maskinlæring i opdagelsen af nye polymererKredit:Tokyo Tech En fælles forskergruppe, herunder Ryo Yoshida (professor og direktør for Data Science Center for Creative Design and Manufacturing ved Institute of Statistical Mathematics [ISM], -
 Klikreaktion for levende systemer:Bioortogonal hydroaminering af aktiverede lineære alkynerKredit:CC0 Public Domain At øge vores forståelse af cellulære processer kræver information om de involverede typer biomolekyler, deres placeringer, og deres interaktioner. Dette kræver, at molekyl
Klikreaktion for levende systemer:Bioortogonal hydroaminering af aktiverede lineære alkynerKredit:CC0 Public Domain At øge vores forståelse af cellulære processer kræver information om de involverede typer biomolekyler, deres placeringer, og deres interaktioner. Dette kræver, at molekyl -
 Ser på molekyler fra to sider med femtosekund bløde røntgenstråler på bordpladenFlydende flatjet (solvatiseret urea) belyst af en bredbånds blød røntgenimpuls opnået ved højordens harmonisk generering. Indsætningerne viser steady-state absorptionen af urinstof ved C- og N K-kan
Ser på molekyler fra to sider med femtosekund bløde røntgenstråler på bordpladenFlydende flatjet (solvatiseret urea) belyst af en bredbånds blød røntgenimpuls opnået ved højordens harmonisk generering. Indsætningerne viser steady-state absorptionen af urinstof ved C- og N K-kan -
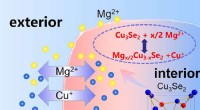 Kobberion låser op for magnesium potentiale i næste generations batterierVed at tilføje en kobberion, nyt magnesiumbatteri demonstrerer dramatisk forbedring af ydeevnen. Kredit:CUI Guanglei Forskere ved Qingdao Institute of Bioenergy and Bioprocess Technology (QIBEBT)
Kobberion låser op for magnesium potentiale i næste generations batterierVed at tilføje en kobberion, nyt magnesiumbatteri demonstrerer dramatisk forbedring af ydeevnen. Kredit:CUI Guanglei Forskere ved Qingdao Institute of Bioenergy and Bioprocess Technology (QIBEBT)
- Hvad betyder udskiller i menneskelig biologi?
- Hvordan demonstrerer celleteorien definition af teori?
- Hvilket objekt konverterer elektricitet til lys?
- Superfonde mærker den økonomiske varme fra klimaforandringerne
- Sort hul spin skruer op for radiovolumen
- Fysikmodeller definerer bedre, hvad der gør pasta 'al dente'


